题目内容
11.下列做法中符合“绿色化学”思想的是( )| A. | CO2不是大气污染物,所以可以大量排放到空气中 | |
| B. | 以无磷洗涤剂代替含磷洗涤剂 | |
| C. | 实验后的有毒有害物质应分类收集,统一处理 | |
| D. | 在通风橱中制取氯气时不用NaOH溶液吸收尾气 |
分析 绿色化学又称环境友好化学,其核心是利用化学原理从源头上减少和消除工业生产对环境的污染,据此解答.
解答 解:A.二氧化碳的大量排放能够引起温室效应,故A错误;
B.含磷洗涤剂的大量使用能够引起水体的富营养化,引起水污染,以无磷洗涤剂代替含磷洗涤剂,可以减少水体的污染,故B正确;
C.实验后的有毒有害物质应分类收集,统一处理,能够减少环境污染,故C正确;
D.在通风橱中制取氯气时不用NaOH溶液吸收尾气,容易引起空气污染,故D错误;
故选:BC.
点评 本题考查了绿色化学的含义,明确绿色化学的要求即可解答,题目难度不大.

练习册系列答案
相关题目
20. 铵盐是一种重要的水体污染物.某课题组利用电解法,在含Cl-的水样中,探究将NH4+转化为N2而脱氮的影响因素和反应机理.
铵盐是一种重要的水体污染物.某课题组利用电解法,在含Cl-的水样中,探究将NH4+转化为N2而脱氮的影响因素和反应机理.
(1)电解法脱氮的原理可能如下:
①直接电氧化
在碱性条件下,发生2NH3+6OH--6e-=N2+6H2O反应的电极为阳极(填“阴”、“阳”)极;
②•OH(羟自由基)电氧化
在电流作用下,利用产生的强氧化性中间产物•OH脱氮;•OH中O元素的化合价-1;
③间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮.请写出HClO在酸性条件下氧化NH4+的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.
(2)探究适宜的实验条件
如图为不同电流强度下脱氮的效果,综合考虑能耗因素,电流强度应选择10A.
(3)该课题组进一步探究脱氮过程中的强氧化性的活性中间产物,提出了如下假设,请你完成假设三:
假设一:只有•OH;
假设二:只有HClO;
假设三:既有•OH又有HClO.
(4)请你设计实验探究脱氮过程中是否有•OH产生,完成下表内容.
(5)研究得知,脱氮过程主要以原理③为主,弱酸性溶液中比强酸溶液中更利于使NH4+转化为N2而脱氮,请从化学平衡移动的角度解释其原因酸性较强时,Cl2+H2O?H++Cl-+HClO的化学平衡逆向移动,生成的HClO减少,不利脱氮.
 铵盐是一种重要的水体污染物.某课题组利用电解法,在含Cl-的水样中,探究将NH4+转化为N2而脱氮的影响因素和反应机理.
铵盐是一种重要的水体污染物.某课题组利用电解法,在含Cl-的水样中,探究将NH4+转化为N2而脱氮的影响因素和反应机理.(1)电解法脱氮的原理可能如下:
①直接电氧化
在碱性条件下,发生2NH3+6OH--6e-=N2+6H2O反应的电极为阳极(填“阴”、“阳”)极;
②•OH(羟自由基)电氧化
在电流作用下,利用产生的强氧化性中间产物•OH脱氮;•OH中O元素的化合价-1;
③间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮.请写出HClO在酸性条件下氧化NH4+的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.
(2)探究适宜的实验条件
如图为不同电流强度下脱氮的效果,综合考虑能耗因素,电流强度应选择10A.
(3)该课题组进一步探究脱氮过程中的强氧化性的活性中间产物,提出了如下假设,请你完成假设三:
假设一:只有•OH;
假设二:只有HClO;
假设三:既有•OH又有HClO.
(4)请你设计实验探究脱氮过程中是否有•OH产生,完成下表内容.
| 实验方案 | 预期实验结果和结论 |
| 配制一定pH、NH4+和Cl-浓度的溶液,用最佳电流强度,电解样品90min后,采用电子自旋共振法检测样品中•OH |
6.下面是同周期元素原子的价电子排布式,第一电离能最小的原子可能是( )
| A. | ns2np3 | B. | ns2np5 | C. | ns2np4 | D. | ns2np6 |
3.实验室可用如图所示装置制取的气体是( )
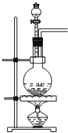

| A. | Cl2 | B. | C2H4 | C. | C2H2 | D. | CO2 |
1.短周期元素X、Y、Z、W、Q在元素周期表中的位置如图所示,其中X元素原子最外层电子数是最内层电子数的3倍,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | X、W分别与钠形成的化合物摩尔质量相同,且每种化合物中阴阳离子数比为1:2 | |
| B. | 含X和Z元素的常见化合物为离子化合物 | |
| C. | 氧化物对应的水化物酸性:W<Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |
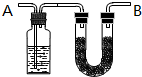 将含有C、H、O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过管A和管B,测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108.
将含有C、H、O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过管A和管B,测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108. .
.