题目内容
19.现有CH4、C2H4、C6H6三种有机物:(1)等质量的三种气体完全燃烧时生成水最多的是CH4;
(2)同状况、同体积的三种气体完全燃烧时耗去O2的量最多的是C2H6.
(3)在150℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是CH4、C2H4.
分析 (1)等质量烃完全燃烧,H元素的质量越大,耗氧量越大;
(2)同状况、同体积的三种气体,其物质的量相等,等物质的量的烃CxHy完全燃烧时,(x+$\frac{y}{4}$)的值越大,耗氧量越大;
(3)在120℃、1.01x105Pa时,烃燃烧生成的水是气态,令烃的平均组成CxHy,根据燃烧反应前后气体体积没有变化,则反应前后气体的化学计量数之和相等,据此根据方程式判断.
解答 解:(1)等质量的烃CxHy完全燃烧时,氢元素的质量分数越大,耗氧量越大,CH4、C2H4、C2H6中的y:x值依次为4、2、3,故CH4中H元素质量分数最大,故等甲烷消耗O2最多,
故答案为:CH4;
(2)同状况、同体积的三种气体,其物质的量相等,等物质的量的烃CxHy完全燃烧时,(x+$\frac{y}{4}$)的值越大,耗氧量越大,CH4、C2H4、C2H6的(x+$\frac{y}{4}$)值依次为1+$\frac{4}{4}$=2、2+$\frac{4}{4}$=3、2+$\frac{6}{4}$=3.5,故C2H6耗O2最多,
故答案为:C2H6;
(3)在105℃、1.01x105Pa时,烃燃烧生成的水是气态,令烃的平均组成CxHy,则:CxHy+(x+$\frac{y}{4}$)O2=xCO2+$\frac{y}{2}$H2O(g),燃烧反应前后气体体积没有变化,则反应前后气体的化学计量数之和相等,故1+(x+$\frac{y}{4}$)=x+$\frac{y}{2}$,解得y=4,即满足H原子数目为4即可,故为CH4、C2H4,
故答案为:CH4、C2H4.
点评 本题考查烃燃烧的有关计算,侧重考查学生分析和解决问题的能力,注意对规律的理解掌握,难度不大.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
8.短周期主族元素X、Y、Z、W在元素周期表中的位置关系如下图,下列推论合理的是( )
| X | Y |
| W | Z |
| A. | 若X、Y、Z、W中只有一种为金属元素,则W一定为铝元素 | |
| B. | 若W的核电荷数是Y的两倍,则W的氧化物可作半导体材料 | |
| C. | 若Z的核电荷数是Y的两倍,则X的氢化物水溶液显酸性 | |
| D. | 若Y、W的简单阴离子都能破坏水的电离,则Z的简单阴离子也一定能破坏水的电离 |
9.下列关于氨水的说法中,不正确的是( )
| A. | 氨水和液氨不同,氨水是混合物,液氨是纯净物 | |
| B. | 氨水中物质的量浓度最大的粒子是NH3•H2O(除水) | |
| C. | 氨水显弱碱性,故通常保存在金属容器中 | |
| D. | 在1 mol•L-1氨水中,NH3•H2O、NH${\;}_{4}^{+}$、NH3的物质的量浓度之和为1 mol•L-1 |
14.X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
| A. | XYZ2 | B. | X2YZ3 | C. | X2YZ2 | D. | XYZ3 |
11.下列做法中符合“绿色化学”思想的是( )
| A. | CO2不是大气污染物,所以可以大量排放到空气中 | |
| B. | 以无磷洗涤剂代替含磷洗涤剂 | |
| C. | 实验后的有毒有害物质应分类收集,统一处理 | |
| D. | 在通风橱中制取氯气时不用NaOH溶液吸收尾气 |
8.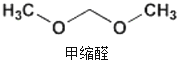 2015年央视3.15晚会曝光了山东省东营市、滨州市许多不法厂商,把一部分90号的汽油配上大量的石脑油、芳烃、甲缩醛等调和成“93号汽油”.查资料知,甲缩醛是一种无色易挥发可燃液体,主要用于生产杀虫剂、皮革和汽车上光剂等,是现行的车用汽油国家标准中不得添加的有害物质,它易造成汽车线路漏油,对动物有麻醉作用,也有一定毒性.下列对其说法中正确的是( )
2015年央视3.15晚会曝光了山东省东营市、滨州市许多不法厂商,把一部分90号的汽油配上大量的石脑油、芳烃、甲缩醛等调和成“93号汽油”.查资料知,甲缩醛是一种无色易挥发可燃液体,主要用于生产杀虫剂、皮革和汽车上光剂等,是现行的车用汽油国家标准中不得添加的有害物质,它易造成汽车线路漏油,对动物有麻醉作用,也有一定毒性.下列对其说法中正确的是( )
 2015年央视3.15晚会曝光了山东省东营市、滨州市许多不法厂商,把一部分90号的汽油配上大量的石脑油、芳烃、甲缩醛等调和成“93号汽油”.查资料知,甲缩醛是一种无色易挥发可燃液体,主要用于生产杀虫剂、皮革和汽车上光剂等,是现行的车用汽油国家标准中不得添加的有害物质,它易造成汽车线路漏油,对动物有麻醉作用,也有一定毒性.下列对其说法中正确的是( )
2015年央视3.15晚会曝光了山东省东营市、滨州市许多不法厂商,把一部分90号的汽油配上大量的石脑油、芳烃、甲缩醛等调和成“93号汽油”.查资料知,甲缩醛是一种无色易挥发可燃液体,主要用于生产杀虫剂、皮革和汽车上光剂等,是现行的车用汽油国家标准中不得添加的有害物质,它易造成汽车线路漏油,对动物有麻醉作用,也有一定毒性.下列对其说法中正确的是( )| A. | 甲缩醛和乙醛互为同系物 | |
| B. | 用甲醇和甲醛生产甲缩醛的反应为加成反应 | |
| C. | 等物质的量的甲缩醛和丙炔完全燃烧的耗氧量相同 | |
| D. | 用甲缩醛生产杀虫剂、皮革和汽车上光剂等,均是利用了它的毒性 |
9.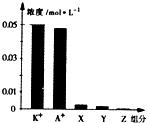 常温下,0.1mol•L-1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.1mol•L-1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
 常温下,0.1mol•L-1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.1mol•L-1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )| A. | 该混合溶液pH=7.0 | B. | 原HA溶液中:c(HA)>c(H+)>c(A-) | ||
| C. | 图中X表示HA,Y表示OH-,Z表示H+ | D. | 混合溶液中:c(X)+x(A-)=c(K+) |
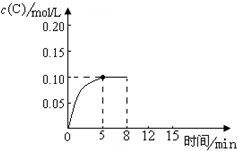 在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)═2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示
在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)═2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示