题目内容
19.t℃时,将 2molSO2 和 1molO2 通入体积为 2L 的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H=-196.6kJ/mol.2min 时反应达到化学平衡,此时测得反应物O2 还剩余 0.8mol,请填写下列空白:(1)从反应开始到达化学平衡,生成 SO3的平均反应速率为0.1mol/(L.min);平衡时,SO2转化率为20%
(2)下列叙述能证明该反应已达到化学平衡状态的是ABE
A.容器内压强不再发生变化 B.SO2 的体积分数不再发生变化
C.容器内气体原子总数不再发生变化 D.相同时间内消耗 2nmolSO2 的同时消耗 nmolO2
E.相同时间内消耗 2nmolSO2的同时生成 nmolO2 F.混合气体密度不再变化
(3)以下操作会引起化学反应速率变快的是ACD
A.向容器中通入O2 B.扩大容器的体积 C.使用正催化剂
D.升高温度 E.向容器中通入氦气.
(4)t2℃时,若将物质的量之比 n(SO2):n(O2)=1:1 的混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了 20%.则SO2的转化率为80%.
分析 (1)t℃时,将 2molSO2 和 1molO2 通入体积为 2L 的恒温恒容密闭容器中,2min 时反应达到化学平衡,此时测得反应物O2 还剩余 0.8mol,则:
2SO2(g)+O2(g)?2SO3(g)
起始量(mol):2 1 0
变化量(mol):0.4 0.2 0.4
平衡量(mol):1.6 0.8 0.4
根据v=$\frac{△c}{△t}$计算v(SO3),平衡时SO2转化率=$\frac{消耗二氧化硫物质的量}{二氧化硫起始物质的量}$×100%;
(2)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
(3)升高温度、使用正催化剂、增大反应物浓度均可以增大反应速率,扩大容器的体积,压强减小,反应速率减慢,恒容条件下通入氦气,反应混合物浓度不变,反应速率不变;
(4)设n(SO2)=n(O2)=1mol,转化的二氧化硫为xmol,则:
2SO2(g)+O2(g)?2SO3(g)
起始量(mol):1 1 0
变化量(mol):x 0.5x x
平衡量(mol):1-x 1-0.5x x
再根据混合气体体积减少了 20%列方程计算解答.
解答 解:(1)t℃时,将 2molSO2 和 1molO2 通入体积为 2L 的恒温恒容密闭容器中,2min 时反应达到化学平衡,此时测得反应物O2 还剩余 0.8mol,则:
2SO2(g)+O2(g)?2SO3(g)
起始量(mol):2 1 0
变化量(mol):0.4 0.2 0.4
平衡量(mol):1.6 0.8 0.4
v(SO3)=$\frac{\frac{0.4mol}{2L}}{2min}$=0.1mol/(L.min),平衡时SO2转化率=$\frac{0.4mol}{2mol}$×100%=20%,
故答案为:0.1mol/(L.min);20%;
(2)A.随反应进行,容器内气体物质的量进行,容器内压强减小,容器内压强不再发生变化说明到达平衡,故A正确;
B.SO2 的体积分数不再发生变化说明到达平衡,故B正确
C.容器内气体原子总数始终不变,故C错误;
D.相同时间内消耗 2nmolSO2 的同时消耗 nmolO2,均表示正反应速率,反应始终按该比例关系进行,故D错误;
E.相同时间内消耗 2nmolSO2的同时生成 nmolO2,而消耗 2nmolSO2的同时消耗 nmolO2,氧气的生成与消耗相等,说明到达平衡,故E正确;
F.混合气体总质量不变,容器容积不变,混合气体密度始终不变,故F错误,
故选:ABE;
(3)A.向容器中通入O2,氧气浓度增大,反应速率加快,故A正确;
B.扩大容器的体积,压强减小,反应速率减慢,故B错误;
C.使用正催化剂,反应速率加快,故C正确;
D.升高温度,反应速率加快,故D正确;
E.恒容条件下通入氦气,反应混合物浓度不变,反应速率不变,故E错误,
故选:ACD;
(4)设n(SO2)=n(O2)=1mol,转化的二氧化硫为xmol,则:
2SO2(g)+O2(g)?2SO3(g)
起始量(mol):1 1 0
变化量(mol):x 0.5x x
平衡量(mol):1-x 1-0.5x x
混合气体体积减少了 20%,则2×20%=2-(1-x+1-0.5x+x),解得x=0.8,平衡时SO2转化率=$\frac{0.8mol}{1mol}$×100%=80%,
故答案为:80%.
点评 本题考查化学平衡计算、平衡状态判断、反应速率计算与影响因素,难度不大,注意对基础知识的理解掌握.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案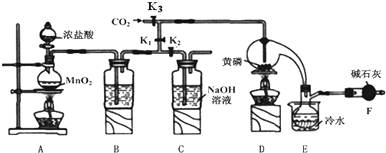
已知:
①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和HC1;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)A装置中制氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O
(2)B中所装试剂是吸收多余的氯气,防止空气中的H2O进入烧瓶和PCl3反应
(3)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O;
(4)F中碱石灰的作用是吸收多余氯气防止污染空气,防止空气中的水蒸气进入烧瓶中与PCl3反应
(5)实验时,检査装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(6)粗产品中常含有POCl3、PCl5等,加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(7)通过下面方法可测定产品中PCl3的质量分数
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3溶液滴定;
④重复②、③操作平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+H2O+I2═H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,假设测定过程中没有其他反应.根据上述数据,该产品中PC13的质量分数为79.75%.
| A. | 0.45mol | B. | 0.8mol | C. | 0.9mol | D. | 1.2mol |
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是df.
a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平 衡 时 数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
| A. | 10mL 18mol/L浓硫酸与足量铜加热充分反应,其中有0.09NA个H2SO4体现了氧化性 | |
| B. | 33.6LCl2一定能与56g铁在加热条件下发生反应 | |
| C. | 12.0g熔融的NaHSO4中含有的阳离子数为0.2NA | |
| D. | 在反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4中,5molFeS2发生反应,有21NA个电子发生转移 |
 O = HIO + HCl 不属于氧化还原反应
O = HIO + HCl 不属于氧化还原反应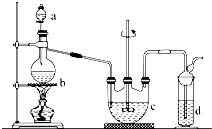 硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它易溶于水,不溶于醇,受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得.实验室模拟该工业过程的装置如图所示.
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它易溶于水,不溶于醇,受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得.实验室模拟该工业过程的装置如图所示. 的路线如图所示.请按要求作答
的路线如图所示.请按要求作答
 .
. ,F
,F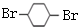 .
. ,
, .
.