题目内容
19.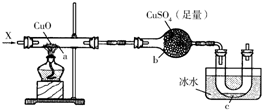 按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,(假设每个反应均完全)
按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,(假设每个反应均完全)(1)则X气体可能是A A.CH3CH2OH B.CO 或 H2 C.NH3
(2)冰水的作用冷凝c处的液体是CH3CHO;
(3)写出试管中反应的化学方程式CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
分析 持续通入X气体或蒸气,可以看到a处有红色物质生成,可知CuO被还原生成Cu,X气体具有还原性;硫酸铜遇水变蓝,b处变蓝,说明有水生成,结合c处得到液体以及题给物质的性质解答该题.
解答 解:(1)A.CH3CH2OH与CuO发生CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+H2O+Cu,可观察到a处有红色物质生成,b处变蓝,c处得到有刺激性气味的液体乙醛,故A正确;
B.CO与CuO反应生成CO2,不能使b处变蓝,故B错误;
C.NH3与CuO反应生成Cu、N2和H2O,可以看到a处有红色物质生成,b处变蓝,但在c出不能得到液体,故C错误;
故答案为:A;
(2)冰水的作用为冷凝,将乙醛气体转化为液体;则c处的液体为CH3CHO,故答案为:冷凝;CH3CHO;
(3)试管中反应的化学方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O,故答案为:CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
点评 本题考查实验装置综合及物质的性质,为高频考点,侧重于学生的分析能力和实验能力的考查,掌握醇的催化氧化的反应原理是解答的关键,答题时注意把握题给信息,题目难度中等.

练习册系列答案
相关题目
9.下列烷烃的系统命名中,不正确的是( )
| A. | 2,3-二甲基戊烷 | B. | 3-甲基-2-乙基己烷 | ||
| C. | 3,3-二甲基戊烷 | D. | 3-甲基-1-丁烯 |
7.据碘与氢气反应的热化学方程式
(1)I2(g)+H2(g)?2HI(g)△H=-9.48 kJ•mol-1
(2)I2(s)+H2(g)?2HI(g)△H=+26.48 kJ•mol-1
下列判断正确的是( )
(1)I2(g)+H2(g)?2HI(g)△H=-9.48 kJ•mol-1
(2)I2(s)+H2(g)?2HI(g)△H=+26.48 kJ•mol-1
下列判断正确的是( )
| A. | 254gI2( g)中通入 2gH2( g),反应放热 9.48 kJ | |
| B. | 1mol固态碘与1mol气态碘所含的能量相差17.00kJ | |
| C. | 反应(1)的产物比反应(2)的产物稳定 | |
| D. | 反应(2)的反应物总能量比反应(1)的反应物总能量低 |
14.1mol某烃完全燃烧可得到2molCO2;在一定条件下,1mol该烃能与1molH2发生加成反应,这种烃是( )
| A. | CH4 | B. | C2H4 | C. | C2H2 | D. | CH3CH2CHO |
11.下列说法不正确的是( )
| A. | 参加反应的物质的性质是决定化学反应速率的主要因素 | |
| B. | 光是影响某些化学反应速率的外界条件之一 | |
| C. | 在给定条件下,当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 | |
| D. | 不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率 |
8.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成.经查资料得知:Ag++2NH3•H2O?Ag(NH3)2++2H2O.下列分析不正确的是( )
| A. | 浊液中存在沉淀溶解平衡:AgCl (s)?Ag+(aq)+Cl-(aq) | |
| B. | 实验可以证明NH3结合Ag+能力比Cl-强 | |
| C. | 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl | |
| D. | 实验表明实验室可用氨水洗涤银镜反应后的试管 |
9.根据表中有关短周期元素性质的数据,判断下列说法中正确的是( )
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | |
| 主要化合价 | 最高价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低价 | -2 | -3 | -1 | -3 | |||||
| A. | ③的熔点低于⑥的熔点 | |
| B. | 元素①与元素⑥形成的化合物皆为碱性氧化物 | |
| C. | 最高价氧化物对应水化物的酸性:⑤>⑦>④ | |
| D. | 元素④形成的氯化物中所有原子周围都达到8电子稳定结构 |
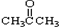 ③CH3CH2Br ④
③CH3CH2Br ④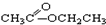 ⑤
⑤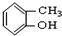 ⑥
⑥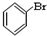 ⑦
⑦ ⑧
⑧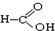 ⑨
⑨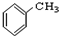 ⑩
⑩