题目内容
8.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成.经查资料得知:Ag++2NH3•H2O?Ag(NH3)2++2H2O.下列分析不正确的是( )| A. | 浊液中存在沉淀溶解平衡:AgCl (s)?Ag+(aq)+Cl-(aq) | |
| B. | 实验可以证明NH3结合Ag+能力比Cl-强 | |
| C. | 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl | |
| D. | 实验表明实验室可用氨水洗涤银镜反应后的试管 |
分析 A、AgCl浊液中存在AgCl的溶解平衡;
B、Ag+与氨气分子结合生成二氨合银离子,导致银离子浓度减小,促使AgCl (s)?Ag+(aq)+Cl-(aq)正向移动;
C、浓硝酸能够中和一水合氨,使反应Ag++2NH3•H2O?Ag(NH3)2++2H2O逆向移动,二氨合银离子生成银离子,与溶液中的氯离子结合;
D、银镜反应后的试管壁上是银单质,其不能和氨水反应.
解答 解:A、因为是浊液,所以存在沉淀溶解平衡,故A正确;
B、Ag+与氨气分子结合生成二氨合银离子,导致银离子浓度减小,促使AgCl (s)?Ag+(aq)+Cl-(aq)正向移动,说明NH3结合Ag+能力比Cl-强,故B正确;
C、浓硝酸能够中和一水合氨,使反应Ag++2NH3•H2O?Ag(NH3)2++2H2O逆向移动,二氨合银离子生成银离子,与溶液中的氯离子结合生成沉淀,所以加浓硝酸后生成的沉淀为AgCl,故C正确;
D、银镜反应后的试管壁上是银单质,银离子能够与氨水反应,银单质不能,故D错误;
故选D.
点评 本题考查了沉淀的溶解平衡的移动,注意银离子能够与氨水反应,银单质不能,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列变化过程中肯定要放出热量的是( )
| A. | C+H20$\frac{\underline{\;\;△\;\;}}{\;}$C0+H2 | B. | H+ → → | ||
| C. | H20(1)→H20(g) | D. | CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ |
3.化学与生产、生活、社会密切相关.下列有关说法中,错误的是( )
| A. | 新农村建设大量使用秸秆制取沼气,符合低碳理念 | |
| B. | 发霉的大米经过石蜡打磨后可以食用和出售 | |
| C. | 2014年西非国家爆发埃博拉病毒,双氧水、高锰酸钾溶液可以完全杀灭该病毒,其消毒原理和漂白粉消毒饮用水相同 | |
| D. | 卤水点豆腐、血液透析、静电除尘都是利用了胶体的性质 |
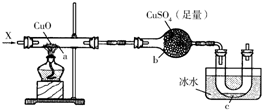 按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,(假设每个反应均完全)
按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,(假设每个反应均完全)

 、
、 、
、
 .
.