题目内容
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+133kJ/mol
H2O(g)=H2O(l)△H=-44kJ/mol
(1)催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为__________________________。
Ⅱ.脱碳:
(2)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)。
CH3OH(l)+H2O(l)。
下列叙述能说明此反应达到平衡状态的是__________。
A.混合气体的平均式量保持不变
B.CO2和H2的体积分数保持不变;
C.CO2和H2的转化率相等
D.混合气体的密度保持不变
E.1molCO2生成的同时有3molH—H键断裂
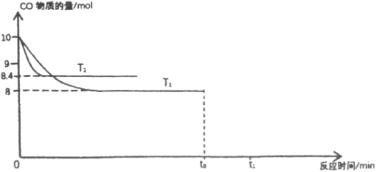
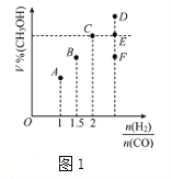
(3)在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,发生反应CO(g)+2H2(g)![]() CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图1所示。
CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图1所示。

①当起始n(H2)/n(CO)=2,经过5min达到平衡,CO的转化率为0.4,则0~5min内平均反应速率V(H2)=__________。若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将__________(选填“增大”、“减小”或“不变”);
②当起始n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图1中的___________点(选填“D”、“E”或“F”)
Ⅲ.脱硫:
如图2所示。
【答案】4H2(g)+2NO2(g)= N2(g)+4H2O(g) △H=-1100.2kJ/mol DE 0.08mol/(L·min) 减小 F
【解析】
(1)依据盖斯定律解答;
(2)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
(3)①建立三段式,依据三段式计算比较;
②合比例等于化学计量数之比时,平衡时生成物的含量最大。
(1)由H2的燃烧热为285.8kJ/mol得①H2(g)+1/2 O2(g)=H2O(l)△H=-285.8KJ/mol,将已知热化学方程式编号为②N2(g)+2O2(g)=2NO2(g)△H=+133kJmol-1,③H2O(g)=H2O(l)△H=-44kJmol-1,由盖斯定律,①×4-②-③×4得到催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJmol-1,故答案为:4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJmol-1;
(2)A、因该反应生成物均为液态,则混合气体的平均式量始终保持不变,不能说明反应达到平衡状态,故A错误;
B、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,所以过程中CO2和H2的体积分数始终保持不变,故B错误;
C、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,CO2和H2的转化率始终相等,不能确定反应是否达到平衡状态,故C错误;
D、反应物是气体,生成物是液体,混合气体的密度保持不变,说明反应达到平衡状态,故D正确;
E、1mol CO2生成的同时有3mol H-H键断裂,说明正逆反应速率相同,反应达到平衡状态,故E正确;
故答案为DE;
(3)①H2和CO总共为3mol,且起始n(H2)/n(CO)=2,可知H2为2mol、CO为1mol,5min达到平衡时CO的转化率为0.4,则由题意建立如下三段式:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始(mol):1 2 0
变化(mol):0.4 0.8 0.4
平衡(mol):0.6 1.2 0.4
容器的容积为2L,则△c(H2)=0.8 mol/2L=0.4mol/L,v(H2)=0.4mol/L/5min=0.08mol/(L·min);该温度下平衡时各物质浓度为c(CO)=0.3 mol/(L·min)、c(H2)=0.6mol/(L·min)、c(CH3OH)=0.2mol/(L·min),则化学平衡常数K=0.2/0.3×0.62,此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,此时浓度商Q=0.4/0.5×0.62>K,反应向逆反应进行,达新平衡时H2的转化率将减小,故答案为:0.08mol/(L.min);减小;
②混合比例等于化学计量数之比时,平衡时生成物的含量最大,故当n(H2)/n(CO)= 3.5时,达到平衡状态后,CH3OH的体积分数小于C点,故答案为:F。

【题目】元素周期表中的四种元素![]() 的有关信息如下,请用合理的化学用语填写空白。
的有关信息如下,请用合理的化学用语填写空白。
在周期表中的区域 | 元素代号 | 有关信息 |
短周期元素 |
|
|
|
| |
长周期元素 |
|
|
|
|
(1)![]() 元素周期表中的位置为___________,
元素周期表中的位置为___________,![]() 、
、![]() 、
、![]() 三种元素的简单离子半径从大到小的顺序为__________。
三种元素的简单离子半径从大到小的顺序为__________。
(2)足量![]() 的最高价氧化物的水化物的稀溶液与
的最高价氧化物的水化物的稀溶液与![]() 甲完全反应,放出热量
甲完全反应,放出热量![]() ,请写出表示该过程中和热的热化学方程式____________。
,请写出表示该过程中和热的热化学方程式____________。
(3)下列有关![]() 的气态氢化物丁的说法正确的有_____________(选填字母)
的气态氢化物丁的说法正确的有_____________(选填字母)
a、丁比氯化氢沸点高 b、丁比氯化氢稳定性好
c、丁比氟化氢还原性强 d、丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式____________;乙的水溶液呈酸性,请写出离子方程式解释原因_____________。
(5)![]() 是一种弱酸,请写出它的电离方程式__________________;
是一种弱酸,请写出它的电离方程式__________________;![]() 溶液有剧毒,可以用
溶液有剧毒,可以用![]() 溶液进行无毒化处理,请写出二者反应的化学方程式__________________;室温下,
溶液进行无毒化处理,请写出二者反应的化学方程式__________________;室温下,![]() 的电离常数
的电离常数![]() ,在
,在![]() 的
的![]() 溶液中滴加同浓度盐酸至溶液呈中性,此时溶液中的
溶液中滴加同浓度盐酸至溶液呈中性,此时溶液中的 _____________。
_____________。