题目内容
【题目】肼![]() 又称联氨,是一种可燃性的液体,可用作火箭燃料。
又称联氨,是一种可燃性的液体,可用作火箭燃料。
![]() 已知在101kPa时,
已知在101kPa时,![]() 时,
时,![]() 在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则
在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则![]() 的燃烧热的热化学方程式是_____________。
的燃烧热的热化学方程式是_____________。
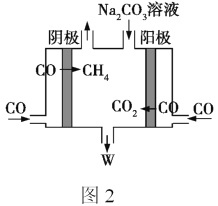
![]() 下图是一个电化学过程示意图。
下图是一个电化学过程示意图。
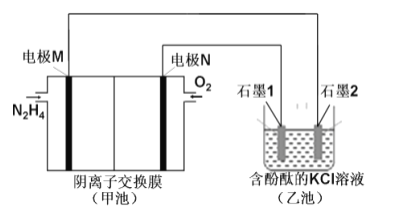
![]() 图中甲池是_________
图中甲池是_________![]() 填“原电池”或“电解池”
填“原电池”或“电解池”![]() ,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
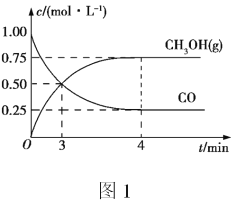
![]() 乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成
乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成![]() 气体时
气体时![]() 标准状况下
标准状况下![]() ,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________
,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________![]() 假设空气中氧气体积含量为
假设空气中氧气体积含量为![]() 。
。
![]() 传统制备肼的方法,是以NaClO氧化
传统制备肼的方法,是以NaClO氧化![]() ,制得肼的稀溶液。该反应的离子方程式是_________。
,制得肼的稀溶液。该反应的离子方程式是_________。
【答案】![]() 原电池
原电池 ![]()
![]()
![]() 28
28 ![]()
【解析】
根据盖斯定律及热化学方程式书写规则计算反应热并书写热化学方程式;根据燃料电池的电极材料判断正负极,并书写电极反应式;根据电解池原理,书写电极反应,并根据电子转移守恒进行相关计算;根据氧化还原反应原理书写并配平氧化还原反应的离子方程式。
![]() 肼的物质的量为10mol,
肼的物质的量为10mol,![]() 在氧气中完全燃烧生成氮气放出热量624kJ,所以其热化学反应方程式为:
在氧气中完全燃烧生成氮气放出热量624kJ,所以其热化学反应方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
![]() ①甲为燃料电池中,负极
①甲为燃料电池中,负极![]() 上投放的是燃料,负极上燃料失电子发生氧化反应,在碱性环境下的反应式为:
上投放的是燃料,负极上燃料失电子发生氧化反应,在碱性环境下的反应式为:![]() ,故答案为:原电池;
,故答案为:原电池;![]() ;
;
②石墨2作电解池的阴极,阴极上氢离子得电子,电极反应式为 ![]() ,当石墨电极2上生成
,当石墨电极2上生成![]() 氢气时,电子转移数为
氢气时,电子转移数为![]() ,整个电路转移1mol电子,根据
,整个电路转移1mol电子,根据![]() 得4mol电子,消耗氧气
得4mol电子,消耗氧气![]() 也就是
也就是![]() ,消耗空气
,消耗空气![]() ,故答案为:
,故答案为:![]() ;
;![]() ;28;
;28;
![]() 氧化
氧化![]() 可以制得肼,根据原子守恒及电荷守恒知,产物中还有Cl-和H2O,则离子方程式为:
可以制得肼,根据原子守恒及电荷守恒知,产物中还有Cl-和H2O,则离子方程式为:![]() ,故答案为:
,故答案为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】下列根据实验及现象得出的结论不正确的是
实验 | 现象 | 结论 | |
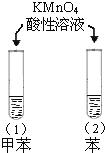
A |
| 试管(1)中紫色消失,试管(2)中紫色没有消失 | 甲苯中苯环使甲基的活性增强 |
B |
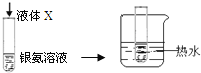
| 试管内壁有银镜生成 | X具有还原性,一定含有醛基 |
C |
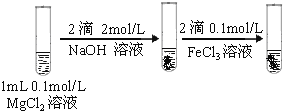
| 先生成白色沉淀,滴加FeCl3溶液后,生成红褐色沉淀 | Fe(OH)3 是比Mg(OH)2 更难溶的电解质 |
D |
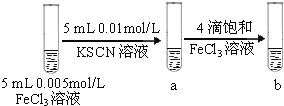
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
A.AB.BC.CD.D