题目内容
【题目】下列根据实验及现象得出的结论不正确的是
实验 | 现象 | 结论 | |
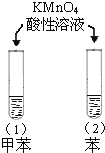
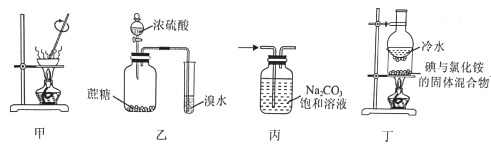
A |
| 试管(1)中紫色消失,试管(2)中紫色没有消失 | 甲苯中苯环使甲基的活性增强 |
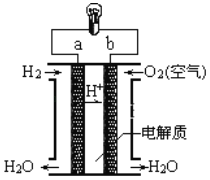
B |
| 试管内壁有银镜生成 | X具有还原性,一定含有醛基 |
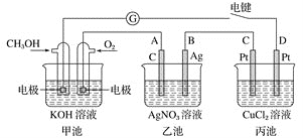
C |
| 先生成白色沉淀,滴加FeCl3溶液后,生成红褐色沉淀 | Fe(OH)3 是比Mg(OH)2 更难溶的电解质 |
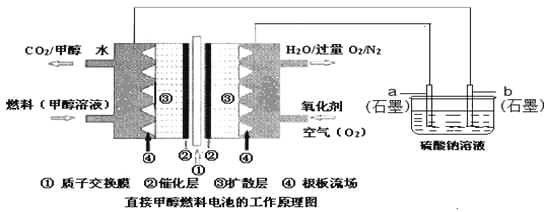
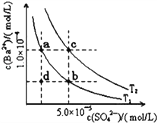
D |
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
A.AB.BC.CD.D
【答案】B
【解析】
A.苯环使甲基变得容易被氧化,故A正确;
B. 试管内壁有银生成,说明X具有还原性,但不一定含有醛基,故B错误;
C.溶解度大的转化成溶解度小的,故C正确;
D. Fe3++3SCN―![]() Fe(SCN)3,增加Fe3+的浓度,平衡正向移动,故D正确;
Fe(SCN)3,增加Fe3+的浓度,平衡正向移动,故D正确;
答案选B。

练习册系列答案
相关题目
【题目】根据要求完成下列各小题:
Ⅰ.(1)理论上稀的强酸、强碱反应生成1molH2O(l)时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式__________________________。
(2)已知:乙苯催化脱氢制苯乙烯反应:![]() +H2(g)
+H2(g)
化学键 | C-H | C-C | C=C | H-H |
键能/kJmol-1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=_________kJmol-1。
Ⅱ.25℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_____________________________。
(2)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:____________________。