题目内容
18.在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )| A. | 2H2(气)+O2(气)═2H2O(气)△H1 2H2(气)+O2(气)═2H2O(液)△H2 | |
| B. | S(气)+O2(气)═SO2(气)△H1 S(固)+O2(气)═SO2(气)△H2 | |
| C. | C(固)+O2(气)═CO2(气)△H1 C(固)+$\frac{1}{2}$O2 (气)═CO(气)△H2 | |
| D. | H2(气)+Cl2(气)═2HCl(气)△H1 $\frac{1}{2}$H2(气)+$\frac{1}{2}$Cl2(气)═HCl(气)△H2 |
分析 A、液态水变为气态水的过程是吸热过程;
B、固体硫变为气态硫需要吸收热量;
C、碳单质完全燃烧放热多于不完全燃烧放的热.
D、化学反应方程式的系数加倍,焓变数值加倍.
解答 解:A、物质的燃烧反应是放热的,所以焓变是负值,液态水变为气态水的过程是吸热的,故△H1>△H2,故A正确;
B、物质的燃烧反应是放热的,所以焓变是负值,固体硫变为气态硫需要吸收热量,所以△H1<△H2,故B错误;
C、碳单质完全燃烧生成二氧化碳放热多于不完全燃烧生成一氧化碳放的热,反应的焓变是负值,故△H1<△H2,故C错误;
D、化学反应方程式的系数加倍,焓变数值加倍,该化合反应是放热的,所以焓变值是负值,2△H1=△H2,△H1<△H2,故D错误;
故选A.
点评 本题考查了物质反应能量变化分析判断,主要是盖斯定律的应用,物质量不同、状态不同、产物不同,反应的能量变化本题,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.关于甲醇碱性燃料电池的叙述正确的是( )
| A. | 加入甲醇的电极是电池的正极 | |
| B. | 电池工作时氧气发生氧化反应 | |
| C. | 电池负极反应式为O2+4H++4e-═2H2O | |
| D. | 电池工作后电解质溶液碱性减弱 |
6. 化学反应的快慢和限度对人类生产生活有重要的意义.
化学反应的快慢和限度对人类生产生活有重要的意义.
(1)将反应速率的影响条件填在空格处.
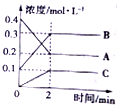
(2)800℃时,A、B、C三种气体在固定体积的密闭容器中反应,反应过程中各物质的浓度变化如图所示,分析图象回答问题:
①该反应的化学方程式为2A?2B+C;
(2)2min内,用C表示的反应速率为0.05mol/(L•min).
③在其他条件下,测得A的反应速率为0.05mol•L-1•min-1,此时的反应与800b℃时相比.
a.比800℃时快 b.比800℃时慢 c.与800℃时速率相等 d.无法确定
(3)判断该反应达到平衡状态的标志是ce
a.A和B的浓度相等
b.v(B)=2v(C)
c.容器内气体压强不再改变
d.密闭容器中混合气体的密度不变
e.容器内A的体积分数不再改变.
 化学反应的快慢和限度对人类生产生活有重要的意义.
化学反应的快慢和限度对人类生产生活有重要的意义.(1)将反应速率的影响条件填在空格处.
| 实例 | 影响条件 |
| ①食物放在冰箱里能延长保质期 | |
| ②工业炼铁时,把铁矿石预先粉碎后,再进行炼制 | |
| ③用H2O2分解制O2,加入MnO2 |
①该反应的化学方程式为2A?2B+C;
(2)2min内,用C表示的反应速率为0.05mol/(L•min).
③在其他条件下,测得A的反应速率为0.05mol•L-1•min-1,此时的反应与800b℃时相比.
a.比800℃时快 b.比800℃时慢 c.与800℃时速率相等 d.无法确定
(3)判断该反应达到平衡状态的标志是ce
a.A和B的浓度相等
b.v(B)=2v(C)
c.容器内气体压强不再改变
d.密闭容器中混合气体的密度不变
e.容器内A的体积分数不再改变.
13.已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H<0.
(1)该反应的化学平衡常数表达式是K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$.
(2)该反应的化学平衡常数K与温度T的关系如下表所示:
其中,K1> K2(填“>”、“=”或“<”).
(3)合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是BD(填字母).
A.用铁触媒加快化学反应速率 B.采用较高压强(20MPa~50MPa)
C.采用较高温度(400℃~500℃) D.将生成的氨液化并及时从体系中分离出来.
(1)该反应的化学平衡常数表达式是K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$.
(2)该反应的化学平衡常数K与温度T的关系如下表所示:
| T/K | 473 | 573 | 673 | … |
| K | 4.4×10-2 | K1 | K2 | … |
(3)合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是BD(填字母).
A.用铁触媒加快化学反应速率 B.采用较高压强(20MPa~50MPa)
C.采用较高温度(400℃~500℃) D.将生成的氨液化并及时从体系中分离出来.
3.在如右图所示的原电池中,下列说法正确的是( )
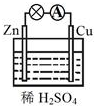

| A. | Zn为负极,Cu为正极 | B. | 正极反应式为:Zn-2e-═Zn2+ | ||
| C. | 负极反应式为:Cu-2e-═Cu2+ | D. | 该装置能将电能转化为化学能 |
10.检验无水乙醇中是否有水的方法是( )
| A. | 加金属钠 | B. | 加入无水硫酸铜 | C. | 加热蒸馏 | D. | 加无水氯化钙 |
8.卤代烃能发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列有机物可以合成环丁烷的是( )
| A. | CH3CH2CH2CH2Br | B. | CH3CH2CHBrCH2CH2Br | ||
| C. | CH2BrCH2CH2CH2Br | D. | CH3CHBrCH2CH2CH2Br |