题目内容
3.关于溶质中微粒间的倍数关系计算:①1mol/L MgCl2溶液,C(Cl-)=2mol/L.
②2mol/L的MgCl2溶液200mL中c(Cl-)=4mol/L,n(Mg2+)=0.8mol.
③0.1mol/L Al2(SO4)3中,Al3+的物质的量浓度为0.2mol/L.
④200mL 0.5mol•L-1 Al2(SO4)3溶液中,c(Al3+)=1mol/L,n(SO${\;}_{4}^{2-}$)=0.3mol.
⑤在aL Na3PO4溶液中,含b mol Na+离子,则此溶液的物质的量浓度为$\frac{b}{3a}$mol/L.
分析 根据n=cV结合物质的构成计算该题.
解答 解:①1mol/L MgCl2溶液,c(Cl-)=2c(MgCl2)=2mol/L,故答案为:2mol/L;
②2mol/L的MgCl2溶液200mL中c(Cl-)=2c(MgCl2)=4mol/L,n(Mg2+)=0.2L×4mol/L=0.8mol,故答案为:4mol/L;0.8mol;
③0.1mol/L Al2(SO4)3中,Al3+的物质的量浓度=2c(Al2(SO4)3)=0.2mol/L,故答案为:0.2mol/L;
④200mL 0.5mol•L-1 Al2(SO4)3溶液中,c(Al3+)=2c(Al2(SO4)3)=1mol/L,n(SO42-)=3×0.2L×0.5mol/L=0.3mol,故答案为:1mol/L;0.3mol;
⑤在aL Na3PO4溶液中,含b mol Na+离子,则n(Na3PO4)=$\frac{b}{3}$mol,此溶液的物质的量浓度为$\frac{b}{3a}$mol/L,故答案为:$\frac{b}{3a}$mol/L.
点评 本题综合考查物质的量浓度的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用以及物质的构成特点,难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
11.有(NH4)2SO4和NH4NO3的混合溶液aL,将它均分成两份,一份滴加KOH溶液,刚好使铵离子全部变为NH3;另一份滴加BaCl2溶液,使SO42-离子完全沉淀,反应中消耗x mol KOH,y molBaCl2,据此得知原混合溶液中的c(NO3-)为( )mol•L-1.
| A. | $\frac{2x-4y}{a}$ | B. | $\frac{2x-y}{a}$ | C. | $\frac{x-2y}{a}$ | D. | $\frac{x-2y}{2a}$ |
18.在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )
| A. | 2H2(气)+O2(气)═2H2O(气)△H1 2H2(气)+O2(气)═2H2O(液)△H2 | |
| B. | S(气)+O2(气)═SO2(气)△H1 S(固)+O2(气)═SO2(气)△H2 | |
| C. | C(固)+O2(气)═CO2(气)△H1 C(固)+$\frac{1}{2}$O2 (气)═CO(气)△H2 | |
| D. | H2(气)+Cl2(气)═2HCl(气)△H1 $\frac{1}{2}$H2(气)+$\frac{1}{2}$Cl2(气)═HCl(气)△H2 |
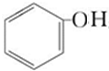 CCH3OH D
CCH3OH D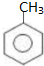 ECH3COOH.
ECH3COOH. .
.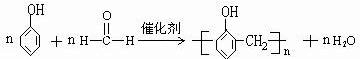 .
.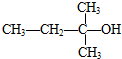 与C的混合物中,在一定温度下使其发生脱水反应,则产物可能有5种.
与C的混合物中,在一定温度下使其发生脱水反应,则产物可能有5种. 反应类型:加聚反应
反应类型:加聚反应 反应类型:取代反应
反应类型:取代反应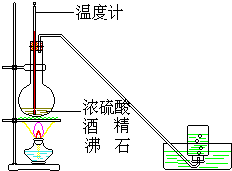 如图是实验室用乙醇与浓硫酸共热制乙烯的实验装置
如图是实验室用乙醇与浓硫酸共热制乙烯的实验装置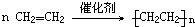 .
.