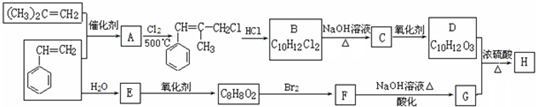
题目内容
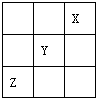
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )

| A、X、Y、Z中X的单质最稳定 |
| B、Y的氢化物为HY |
| C、Z的最高价氧化物的化学式为ZO2 |
| D、能发生Cl2+H2Z═Z+2HCl的反应 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:这几种元素都是短周期元素,根据元素在周期表中的位置知,X是He元素、Y是F元素、Z是S元素,
A.稀有气体单质最稳定;
B.Y在化合物中显-1价,根据化合物中化合价的代数和为0确定其氢化物化学式;
C.Z的最高化合价是+6价,根据化合物中化合价的代数和为0确定其最高价氧化物的化学式;
D.氯气具有强氧化性,能置换出硫化氢溶液中的硫单质.
A.稀有气体单质最稳定;
B.Y在化合物中显-1价,根据化合物中化合价的代数和为0确定其氢化物化学式;
C.Z的最高化合价是+6价,根据化合物中化合价的代数和为0确定其最高价氧化物的化学式;
D.氯气具有强氧化性,能置换出硫化氢溶液中的硫单质.
解答:
解:这几种元素都是短周期元素,根据元素在周期表中的位置知,X是He元素、Y是F元素、Z是S元素,
A.稀有气体元素最外层达到稳定结构,不容易失去电子和得到电子,所以这三种单质最稳定的是He,故A正确;
B.Y在化合物中显-1价,根据化合物中化合价的代数和为0确定其氢化物化学式为HY,故B正确;
C.Z的最高化合价是+6价,根据化合物中化合价的代数和为0确定其最高价氧化物的化学式为SO3,故C错误;
D.同一周期元素,非金属性随着原子序数增大而增强,元素的非金属性越强,其单质的氧化性越强,所以氯气氧化性大于S,氯气能置换出硫化氢溶液中的硫单质,故D正确;
故选C.
A.稀有气体元素最外层达到稳定结构,不容易失去电子和得到电子,所以这三种单质最稳定的是He,故A正确;
B.Y在化合物中显-1价,根据化合物中化合价的代数和为0确定其氢化物化学式为HY,故B正确;
C.Z的最高化合价是+6价,根据化合物中化合价的代数和为0确定其最高价氧化物的化学式为SO3,故C错误;
D.同一周期元素,非金属性随着原子序数增大而增强,元素的非金属性越强,其单质的氧化性越强,所以氯气氧化性大于S,氯气能置换出硫化氢溶液中的硫单质,故D正确;
故选C.
点评:本题考查了元素周期表和元素周期律综合应用,根据元素位置确定元素,再结合物质结构、元素周期律分析解答,知道主族元素最高正化合价与族序数关系,题目难度不大.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,只用一种试剂并通过一步实验就能加以区别.这种试剂是( )
| A、AgNO3 |
| B、NaOH |
| C、H2SO4 |
| D、BaCl2 |
化学学习方法中的类推法是由已学知识通过迁移构建新知识的方法.下列类比正确的是( )
| A、锌可以写溶液中的银离子发生置换反应,钠也能与溶液中的银离子发生置换反应 |
| B、钠与乙醇反应产生氢气,钾与乙醇也能反应产生氢气 |
| C、铜在氯气中剧烈燃烧生成二价铜,铜也能在硫蒸气中剧烈燃烧生成二价铜 |
| D、铜与浓硝酸可以制取NO2,常温下铁与浓耙酸也可以制取NO2 |
下列化学用语正确的是( )
A、氯化氢的电子式: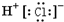 |
B、镁的原子结构示意图: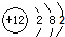 |
| C、乙酸的结构简式 C2H4O2 |
| D、碳酸钠的电离方程式 NaHCO3═Na++H++CO32- |
实验中安全意识是重要的科学素养,下列实验操作或事故的处理操作正确的是( )
| A、可以用饱和溴水除去苯中混有的苯酚 |
| B、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| C、中和滴定时,应用待测液润洗滴定管和锥形瓶 |
| D、做完铜和浓硫酸反应的大试管实验结束时要立即往试管中加水清洗,这样可以减少尾气的产生 |
将0.5mol Na投入过量的水(m1g)中,得到a g溶液;将0.5mol Zn投入过量的盐酸(m2g)中,得到bg溶液,若m1═m2,则a.b的质量关系是( )
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
下列离子方程式中正确的是( )
| A、碳酸氢铵溶液与足量苛性钾溶液混合共热:NH4++OH-=NH3↑+H2O |
| B、Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、往硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-=CuS↓+H2S↑ |
| D、石灰石溶解在醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |