题目内容
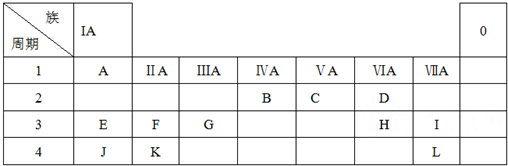
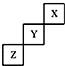
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )

| A、X、Y、Z三种元素中,单质在常温下均为气态 |
| B、Z的氢化物的稳定性比Y的强 |
| C、Y的最高正化合价为+5 |
| D、Y的单质的熔点比Z的低 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素X、Y、Z在元素周期表中的位置可知,X为He、Y为F、Z为S,结合元素单质性质与元素周期律解答.
解答:
解:由短周期元素X、Y、Z在元素周期表中的位置可知,X为He、Y为F、Z为S,
A.常温下,氦气、氟气为气态,硫为固体,故A错误;
B.非金属性F>S,故氢化物稳定性HF>H2S,故B错误;
C.Y为F元素,没有正化合价,故C错误;
D.常温下,氟气为气态,硫为固体,故单质硫的熔点较高,故D正确,
故选D.
A.常温下,氦气、氟气为气态,硫为固体,故A错误;
B.非金属性F>S,故氢化物稳定性HF>H2S,故B错误;
C.Y为F元素,没有正化合价,故C错误;
D.常温下,氟气为气态,硫为固体,故单质硫的熔点较高,故D正确,
故选D.
点评:本题考查元素周期表与元素周期表,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
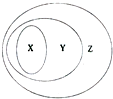 如图表示了x、y、z事物间的从属关系,下列选项中不符合图中事物间从属关系的是( )
如图表示了x、y、z事物间的从属关系,下列选项中不符合图中事物间从属关系的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 中和反应 | 复分解反应 | 化学反应 |
| B | 电解质 | 盐 | 化合物 |
| C | 胶体 | 分散系 | 混合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
下列叙述正确的是( )
| A、黄铜属于合金,硬度比纯铜高 |
| B、MgO、Al2O3是耐高温材料,工业上常用其电解冶炼对应的金属 |
| C、二氧化硫具有漂白性,与氯水混合使用漂白效果更好 |
| D、金属单质与盐溶液的反应都是置换反应 |
下列事实不能用勒夏特列原理解释的是( )
| A、工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B、合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率 |
| C、过氧化氢分解加二氧化锰作催化剂,使单位时间内产生的氧气的量多 |
| D、久制的氯水PH值变小 |
反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )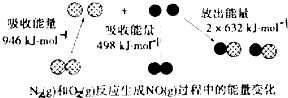
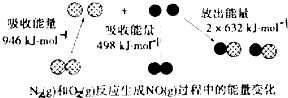
| A、通常情况下,N2(g)和O2(g)混合能直接生成NO |
| B、1mol N2(g)和NA个O2(g)反应放出的能量为180kJ |
| C、NO是一种酸性氧化,能与NaOH溶液反应生成盐和水 |
| D、1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 |
钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的是( )
| A、K可以与水剧烈反应,生成氢气 |
| B、K在空气可以被氧化,产物是K2O2 |
| C、K可以在空气中燃烧,产物是K2O2 |
| D、因为K的活泼性比钠强,所以钠不能置换出钾 |
已知破坏1mol H-H键、Cl-Cl键、H-Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与Cl2生成1mol HCl总的过程需要( )
| A、放热185 kJ |
| B、吸热185 kJ |
| C、放热92.5 kJ |
| D、吸热92.5 kJ |
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,只用一种试剂并通过一步实验就能加以区别.这种试剂是( )
| A、AgNO3 |
| B、NaOH |
| C、H2SO4 |
| D、BaCl2 |