题目内容
下列化学反应的离子方程式其中正确的是( )
| A、铁与氯化铁溶液反应:Fe+2Fe3+═3Fe2+ |
| B、氨水与盐酸反应:OH-+H+═H2O |
| C、氢氧化钡溶液与硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| D、碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成氯化亚铁;
B.弱电解质写化学式;
C.水分子的计量数是2;
D.难溶物写化学式.
B.弱电解质写化学式;
C.水分子的计量数是2;
D.难溶物写化学式.
解答:
解:A.二者反应生成氯化亚铁,离子方程式为Fe+2Fe3+═3Fe2+,故A正确;
B.弱电解质写化学式,离子方程式为NH3.H2O+H+=NH4++H2O,故B错误;
C.水分子的计量数是2,离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.难溶物写化学式,离子方程式为CaCO3+2H+═CO2↑+H2O+Ca2+,故D错误;
故选A.
B.弱电解质写化学式,离子方程式为NH3.H2O+H+=NH4++H2O,故B错误;
C.水分子的计量数是2,离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.难溶物写化学式,离子方程式为CaCO3+2H+═CO2↑+H2O+Ca2+,故D错误;
故选A.
点评:本题考查了离子方程式的书写,明确物质之间的反应及离子方程式书写规则即可解答,弱电解质、单质、氧化物、气体、沉淀、络合物等都要写化学式.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
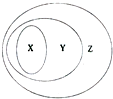 如图表示了x、y、z事物间的从属关系,下列选项中不符合图中事物间从属关系的是( )
如图表示了x、y、z事物间的从属关系,下列选项中不符合图中事物间从属关系的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 中和反应 | 复分解反应 | 化学反应 |
| B | 电解质 | 盐 | 化合物 |
| C | 胶体 | 分散系 | 混合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的是( )
| A、K可以与水剧烈反应,生成氢气 |
| B、K在空气可以被氧化,产物是K2O2 |
| C、K可以在空气中燃烧,产物是K2O2 |
| D、因为K的活泼性比钠强,所以钠不能置换出钾 |
已知破坏1mol H-H键、Cl-Cl键、H-Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与Cl2生成1mol HCl总的过程需要( )
| A、放热185 kJ |
| B、吸热185 kJ |
| C、放热92.5 kJ |
| D、吸热92.5 kJ |
下列说法正确的是( )
| A、蛋白质都是结构复杂的高分子化合物,分子中都含有C、H、O、N等四种元素 |
| B、油脂在一定条件能发生水解反应,属于高分子 |
| C、棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| D、“蜡烛成灰泪始干”中的“泪”主要是有机烯烃 |
9g二氧化碳和一氧化碳组成的混合气体与一定量O2恰好完全反应后得到二氧化碳5.6L(标准状况),下列说法正确的是( )
| A、反应前CO和CO2的体积比为1:1 |
| B、反应前CO和CO2的质量比为1:1 |
| C、反应前CO和CO2的混合气体与反应后气体体积比(同温同压下)为1:2 |
| D、反应前CO和CO2的混合气体与反应后气体所含氧原子的个数比为1:2 |
下列除杂质的方法正确的是( )
| A、用铁粉除去FeCl3溶液中少量的CuCl2 |
| B、用饱和碳酸钠溶液除去CO2中少量的SO2气体 |
| C、用过量的碱液除去H2中少量的HCl气体 |
| D、用过量的氨水除去Al3+溶液中的少量Fe3+ |
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,只用一种试剂并通过一步实验就能加以区别.这种试剂是( )
| A、AgNO3 |
| B、NaOH |
| C、H2SO4 |
| D、BaCl2 |
化学学习方法中的类推法是由已学知识通过迁移构建新知识的方法.下列类比正确的是( )
| A、锌可以写溶液中的银离子发生置换反应,钠也能与溶液中的银离子发生置换反应 |
| B、钠与乙醇反应产生氢气,钾与乙醇也能反应产生氢气 |
| C、铜在氯气中剧烈燃烧生成二价铜,铜也能在硫蒸气中剧烈燃烧生成二价铜 |
| D、铜与浓硝酸可以制取NO2,常温下铁与浓耙酸也可以制取NO2 |