题目内容
工业上合成甲醇一般采用下列反应:CO(g)+2H(g)?CH30H(g)△H<0,下表是该反应在不同温度下的化学平衡常数(K):
则下列数据符合表中x的是( )
| 温度/℃ | 250 | 350 |
| K/(mol?L-2)-2 | 2.041 | x |
| A、0 | B、0.012 |
| C、32.081 | D、100 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:反应是气体体积减小的放热反应,温度升高平衡逆向进行,平衡常数减小;
解答:
解:CO(g)+2H(g)?CH30H(g)△H<0,反应是气体体积减小的放热反应,温度升高平衡逆向进行,平衡常数减小,小于2.041,反应是可逆反应,但不能为0;
故选B.
故选B.
点评:本题考查了平衡常数影响因素分析,注意平衡常数随温度变化,平衡移动原理理解是关键,题目较简单.

练习册系列答案
相关题目
已知破坏1mol H-H键、Cl-Cl键、H-Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与Cl2生成1mol HCl总的过程需要( )
| A、放热185 kJ |
| B、吸热185 kJ |
| C、放热92.5 kJ |
| D、吸热92.5 kJ |
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,只用一种试剂并通过一步实验就能加以区别.这种试剂是( )
| A、AgNO3 |
| B、NaOH |
| C、H2SO4 |
| D、BaCl2 |
下列与实验相关的叙述正确的是( )
| A、测定中和热时,应将NaOH溶液分次缓慢倒入装有盐酸的烧杯中,并搅拌 |
| B、配置溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、酸碱滴定时,若加入待测前用待测液润洗锥形瓶,将导致测定结果偏高 |
| D、检验某溶液是否含有SO42-时,应取少量溶液,依次加入BaCl2溶液和稀盐酸 |
下列有关化学键与晶体结构说法正确的是( )
| A、原子晶体中共价键越强,熔点越高 |
| B、金属元素和非金属元素形成的化合物一定是离子化合物 |
| C、含有阴离子的化合物一定含有阳离子 |
| D、分子晶体中分子间作用力越大,分子越稳定 |
常温下,0.01mol?L-1 MOH溶液的pH为10.已知:
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
| A、+33.1kJ?mol-1 |
| B、+45.2kJ?mol-1 |
| C、-81.5kJ?mol-1 |
| D、-33.1kJ?mol-1 |
化学学习方法中的类推法是由已学知识通过迁移构建新知识的方法.下列类比正确的是( )
| A、锌可以写溶液中的银离子发生置换反应,钠也能与溶液中的银离子发生置换反应 |
| B、钠与乙醇反应产生氢气,钾与乙醇也能反应产生氢气 |
| C、铜在氯气中剧烈燃烧生成二价铜,铜也能在硫蒸气中剧烈燃烧生成二价铜 |
| D、铜与浓硝酸可以制取NO2,常温下铁与浓耙酸也可以制取NO2 |
下列化学用语正确的是( )
A、氯化氢的电子式: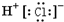 |
B、镁的原子结构示意图: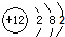 |
| C、乙酸的结构简式 C2H4O2 |
| D、碳酸钠的电离方程式 NaHCO3═Na++H++CO32- |