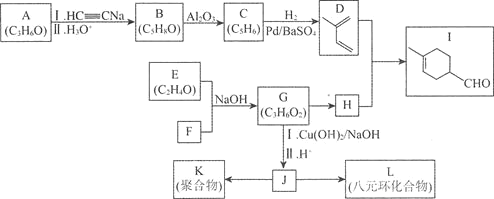
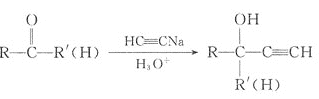
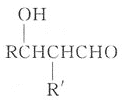
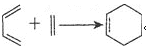
题目内容
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )

A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,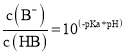
【答案】C
【解析】
A.当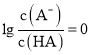 时,
时,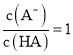 ,
,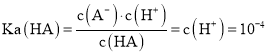 ,同理
,同理![]() ,相同温度下,酸的电离平衡常数越大,酸的酸性越强,因为
,相同温度下,酸的电离平衡常数越大,酸的酸性越强,因为![]() ,所以酸性
,所以酸性![]() ,故A正确;
,故A正确;
B.b点时,横坐标为0,则![]() ,溶液
,溶液![]() ,溶液呈酸性,则
,溶液呈酸性,则![]() ,溶液中存在电荷守恒,根据电荷守恒得
,溶液中存在电荷守恒,根据电荷守恒得![]() ,溶液中
,溶液中![]() 较小,所以存在
较小,所以存在![]() ,故B正确;
,故B正确;
C.根据A知,酸性![]() ,则水解程度
,则水解程度![]() ,所以相同浓度相同体积的NaA和NaB溶液中
,所以相同浓度相同体积的NaA和NaB溶液中![]() :
:![]() ,温度相同水的离子积常数相同,则这两种溶液中
,温度相同水的离子积常数相同,则这两种溶液中![]() :
:![]() ,溶液中分别存在电荷守恒
,溶液中分别存在电荷守恒![]() 、
、![]() ,根据物料守恒得两种溶液中
,根据物料守恒得两种溶液中![]() 相等,所以
相等,所以![]() :
:![]() ,根据电荷守恒知,阴离子浓度总数
,根据电荷守恒知,阴离子浓度总数![]() ,故C错误;
,故C错误;
D.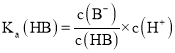 ,则
,则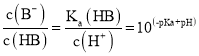 ,故D正确;
,故D正确;
答案选C。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】重铬酸钾(K2Cr2O7)为用途极广的铬化合物,供制铬矾。火柴、铬颜料、并供鞣革、电镀、有机合成等用。铬铁矿的主要成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备K2Cr2O7晶体的过程如图所示:
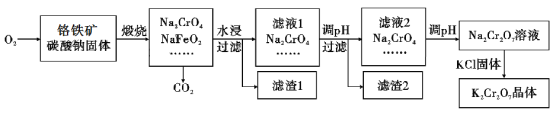
根据题意回答下列问题:
(1)锻烧时,铬铁矿发生复杂反应生成Na2CrO4和NaFeO2,同时杂质SiO2、Al2O3与Na2CO3发生反应,其中Al2O3发生反应的化学方程式是___。
(2)NaFeO2遇水强烈水解生成滤渣l的反应离子方程式是___。
(3)滤液1和滤液2均需调节溶液pH,滤液1调节pH为7-8目的是___,滤液2调节pH约为5目的是___。
物质 | 溶解度/(g/100g水) | ||
0℃ | 40℃ | 80℃ | |
KCl | 28 | 40.1 | 51.3 |
NaCl | 35.7 | 36.4 | 38 |
K2Cr2O7 | 4.7 | 26.3 | 73 |
Na2Cr2O7 | 163 | 215 | 376 |
(4)向Na2Cr2O7溶液中加入KCl固体,析出K2Cr2O7晶体。此法能够制得K2Cr2O7晶体的原因是:___;为了从溶液中得到较多K2Cr2O7晶体的操作过程是:___、过滤、洗涤、干燥。将得到的K2Cr2O7晶体进一步纯化操作是:___。
(5)K2Cr2O7性质:往K2Cr2O7溶液中加入AgNO3溶液,生成一种砖红色沉淀、溶液的pH减小,反应离子方程式是___。
(6)K2Cr2O7产品含量测定:准确称取试样2.5g配成250mL溶液,用移液管吸取25.00mL溶液放入碘量瓶,加入10mL2mol/L硫酸、2gKI于暗处5min,另加100mL水,用0.2000mol/L Na2S2O3标准液滴定至溶液黄绿色,再加3mL淀粉溶液继续滴定至蓝色褪去并呈亮绿色。平行三次实验,平均消耗Na2S2O3标准液的体积25.00mL。K2Cr2O7产品的纯度为___。
有关反应如下:K2Cr2O7+6KI+7H2SO4=Cr2(SO4)3+4K2SO4+3I2+7H2O
2Na2S2O3+I2=Na2S4O6+2NaI