题目内容
【题目】二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g);ΔH=-246.4 kJ·mol-1 它可以分为两步,反应分别如下:
CH3OCH3(g)+CO2(g);ΔH=-246.4 kJ·mol-1 它可以分为两步,反应分别如下:
①4H2(g)+2CO(g)===CH3OCH3(g)+H2O(g), ΔH1=-205.1 kJ·mol-1
②CO(g)+H2O(g)===CO2(g)+H2(g);ΔH2=________。
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO转化率的是________(填字母代号)。
A.降低温度 B.加入催化剂
C.缩小容器体积 D.增加H2的浓度
E.增加CO的浓度
(3)在一体积可变的密闭容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,在一定温度和压强下发生反应:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
问:①反应开始时正、逆反应速率的大小:v(正)______(填“>”、“<”或“=”)v(逆)。
②平衡时n(CH3OCH3)=________,平衡时CO的转化率=________。
【答案】-41.3KJ/mol CD > 1.75 75%
【解析】
根据题意可知,本题考查焓变的计算、转化率大小和计算及反应速率的大小比较,运用盖斯定律,勒夏特列原理分析。
(1)③3H2(g)+3CO(g)CH3OCH3(g)+CO2(g)ΔH=-246.4 kJ·mol-1;①4H2(g)+2CO(g)===CH3OCH3(g)+H2O(g)ΔH1=-205.1 kJ·mol-1;②CO(g)+H2O(g)===CO2(g)+H2(g)ΔH2;由盖斯定律:①+②=③可得:ΔH=ΔH1+ΔH2=-205.1kJ·mol-1+ΔH2=-246.4 kJ·mol-1,解得ΔH2=-41.3 kJ·mol-1;
故答案为:-41.3 kJ·mol-1;
(2)A.正反应为放热反应,降低温度,平衡向正反应方向移动,CO的转化率增大,但反应速率减小,故A错误;
B.加入催化剂,反应速率增大,不影响平衡移动,CO的转化率不变,故B错误;
C.正反应为气体体积减小的反应,缩小容器体积,压强增大,反应速率增大,平衡向正反应方向移动,CO的转化率增大,故C正确;
D.增加H2的浓度,反应速率增大,平衡向正反应移动,CO的转化率增大,故D正确;
E.增加CO的浓度,反应速率增大,平衡向正反应移动,但CO的转化率减小,故E错误;
故答案为:CD;
(3)①同温同压下,气体密度之比等于平均相对分子质量之比,平衡时混合气体密度增大,说明混合气体物质的量减小,反应正向进行建立平衡,故v(正)>v(逆);
故答案为:>;
②平衡时混合气体密度是同温同压下起始时的1.6倍,则平衡时混合气体物质的量为(3mol+3mol+1mol+1mol)×![]() =5mol,则:
=5mol,则:
故平衡时n(CH3OCH3)=1.75mol,平衡时CO的转化率为为![]() ;
;
故答案为:1.75mol;75%。

【题目】甲、乙两个实验小组利用![]() 酸性溶液与
酸性溶液与![]() 溶液反应研究影响反应速率的因素。
溶液反应研究影响反应速率的因素。
设计实验方案如下![]() 实验中所用
实验中所用![]() 溶液均已加入
溶液均已加入![]() :
:
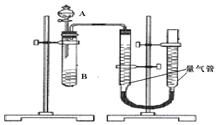
甲组:通过测定单位时间内生成![]() 气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
序号 | A溶液 | B溶液 |
① |
|
|
② |
|
|
③ |
|
|
![]() 该反应的离子方程式为 ______
该反应的离子方程式为 ______
![]() 实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入
实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入![]() 填“一次性”或“逐滴滴加”
填“一次性”或“逐滴滴加”![]()
![]() 完成该实验还需要 ______
完成该实验还需要 ______ ![]() 填仪器名称
填仪器名称![]() ,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
乙组:通过测定![]() 溶液褪色所需时间的多少来比较化学反应速率为了探究
溶液褪色所需时间的多少来比较化学反应速率为了探究![]() 与
与![]() 浓度对反应速率的影响,某同学在室温下完成以下实验
浓度对反应速率的影响,某同学在室温下完成以下实验
实验编号 | 1 | 2 | 3 | 4 |
水 | 10 | 5 | 0 | X |
| 5 | 10 | 10 | 5 |
| 5 | 5 | 10 | 10 |
时间 | 40 | 20 | 10 | --- |
![]() ______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
![]() 号反应中,
号反应中,![]() 的反应速率为 ______。
的反应速率为 ______。
![]() 在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
温度℃ | 25 | 26 | 26 | 26 |
| 27 | 27 |
结合实验目的与表中数据,你得出的结论是 ______。
![]() 从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______
从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______ ![]() 填字母
填字母![]() 。
。
A 硫酸钾![]() 水
水![]() 二氧化锰
二氧化锰![]() 硫酸锰。
硫酸锰。