题目内容
6.下列有关氮元素及其化合物的表示正确的是( )| A. | 质子数为7、中子数为7的氮原子:${\;}_{7}^{7}$N | |
| B. | 氮离子(N3-)的结构示意图: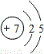 | |
| C. | 氨气分子的电子式: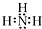 | |
| D. | 甘氨酸分子的结构简式:C2H5O2N |
分析 A.质量数=质子数+中子数,元素符号的左上角表示质量数,左下角表示质子数;
B.氮离子的核电荷数为7,最外层电子数为8;
C.氨气为共价化合物,其分子中含有3个N-H键;
D.结构简式中应该标出有机物官能团机构.
解答 解:A.质子数为7、中子数为7的氮原子的质量数为14,该原子的正确表示方法为:147N,故A错误;
B.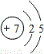 为氮原子结构示意图,氮离子的最外层电子数为8,氮离子正确的离子结构示意图为
为氮原子结构示意图,氮离子的最外层电子数为8,氮离子正确的离子结构示意图为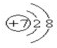 ,故B错误;
,故B错误;
C.氨气分子中,氮原子最外层达到8电子稳定结构,氨气分子的电子式为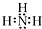 ,故C正确;
,故C正确;
D.C2H5O2N为分子式,甘氨酸的结构简式为:H2NCH2COOH,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、元素符号、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
1.下列图示与对应的叙述相符的是( )
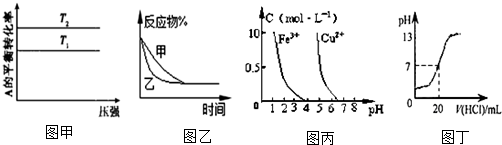

| A. | 图甲可以判断出反应 A(g)+B(g)?2C(g) 的△H<0,T2>T1 | |
| B. | 图乙表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 | |
| C. | 据图丙,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH≈4.5 | |
| D. | 图丁表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入盐酸体积的变化 |
11.在给定条件下,下列选项中所示的物质间转化不能一步实现的是( )
| A. | FeS2$\stackrel{O_{2}/高温}{→}$SO2$\stackrel{H_{2}O_{2}(aq)}{→}$H2SO4 | |
| B. | 饱和NaCl溶液$\stackrel{NH_{3},CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | CuSO4(aq)$\stackrel{过量NaOH(aq)}{→}$Cu(OH)2$\stackrel{葡萄糖(aq)/△}{→}$Cu2O | |
| D. | 1 mol•L-1HCl(aq)$\stackrel{MnO_{2}/△}{→}$Cl2$\stackrel{石灰乳}{→}$Ca(ClO)2 |
15.已知合成氨的反应为:N2+3H2═2NH3 △H=-92.4KJ/mol在一定条件下达到化学平衡,现升高温度使平衡发生移动,下列图象中能正确描述正、逆反应速率(v)变化的是( )
| A. | 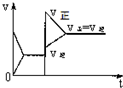 | B. | 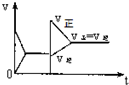 | C. | 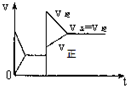 | D. | 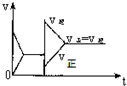 |
16.用浓盐酸和二氧化锰制氯气的实验装置如图所示:
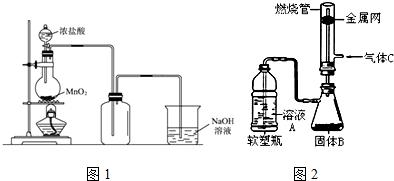
(1)制得的氯气中还含有氯化氢杂质,可通过装有饱和食盐水的洗气瓶除去.
(2)二氧化锰和高锰酸钾都是强氧化剂,均可将浓盐酸氧化为氯气.用浓盐酸和高锰酸钾制氯气的反应方程式如下:2KMnO4+16HCl2KCl+2 MnCl2+5 Cl2+8 H2O
①配平该反应的化学方程式.
②当有1mol电子转移时,被氧化的HCl1mol,可生成气体(标准状态下)11.2 L.
(3)有人做了一个改进实验.挤压软塑料瓶,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并在管口点燃,可以看到可燃性气体C有明显的燃烧现象(金属网用以防止气体混合爆炸).用此装置模拟工业合成盐酸.则相应试剂选择正确的是c(选填序号).
管口可观察到的现象是苍白色火焰,管口上方有白雾.

(1)制得的氯气中还含有氯化氢杂质,可通过装有饱和食盐水的洗气瓶除去.
(2)二氧化锰和高锰酸钾都是强氧化剂,均可将浓盐酸氧化为氯气.用浓盐酸和高锰酸钾制氯气的反应方程式如下:2KMnO4+16HCl2KCl+2 MnCl2+5 Cl2+8 H2O
①配平该反应的化学方程式.
②当有1mol电子转移时,被氧化的HCl1mol,可生成气体(标准状态下)11.2 L.
(3)有人做了一个改进实验.挤压软塑料瓶,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并在管口点燃,可以看到可燃性气体C有明显的燃烧现象(金属网用以防止气体混合爆炸).用此装置模拟工业合成盐酸.则相应试剂选择正确的是c(选填序号).
| 溶液A | 固体B | 气体C | |
| a | 稀硫酸 | Zn | Cl2 |
| b | 浓盐酸 | MnO2 | H2 |
| C | 浓盐酸 | KMnO4 | H2 |
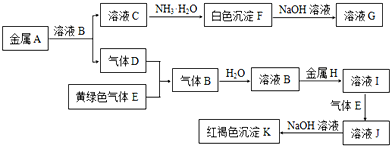
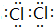 ,G的化学式是NaAlO2.
,G的化学式是NaAlO2.