题目内容
17.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).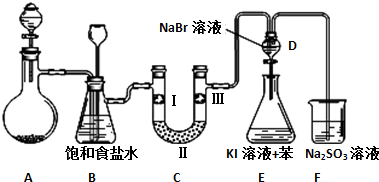
(1)制备氯气选用的药品为漂粉精固体和浓盐酸,相关的化学反应方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl,同时装置B亦是安全瓶,可用来监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是d(填编号);
| 编号 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)从原子结构角度解释氯、溴、碘的非金属性强弱递变规律及原因氯、溴、碘同主族,从上到下,原子半径逐渐增大,得电子能力减弱,元素非金属性减弱;
(6)装置F的目的是吸收余氯,试写出相应的离子反应方程式SO32-+Cl2+H2O=SO42-+2Cl-+2H+.
分析 (1)次氯酸钙常温下能够氧化浓盐酸,反应生成氯化钙、氯气和水;
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,要得到纯净的氯气应除去氯气中的氯化氢;
依据C发生堵塞时,B中压强增大,分析解答;
(3)验证氯气是否具有漂白性,则先设计湿润的有色物质,再利用干燥剂干燥后与干燥的有色物质混合;
(4)D、E的目的是比较氯、溴、碘的非金属性,D中发生氯气与NaBr的反应生成溴,打开活塞,将装置D中少量溶液加入装置E中,氯气、溴均可与KI反应生成碘,单质碘易溶于苯而显紫红色;
(5)依据同主族元素原子半径从上到下依次增大,得电子能量逐渐减弱,元素非金属性减弱解答;
(6)亚硫酸钠具有强的还原性与氯气反应氧化还原反应生成硫酸钠和盐酸.
解答 解:(1)次氯酸钙常温下能够氧化浓盐酸,反应生成氯化钙、氯气和水,化学方程式:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
故答案为:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,用B装置可以除去氯气中的氯化氢气体;
装置B是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的压强增大,锥形瓶中液面下降,长颈漏斗中液面上升;
故答案为:除去Cl2中的HCl; B中长颈漏斗中液面上升,形成水柱;
(3)验证氯气是否具有漂白性,则先通过I中湿润的有色布条,观察到褪色,再利用II中固体干燥剂(无水氯化钙或硅胶)干燥后,在Ⅲ中放入干燥的有色布条,观察到颜色不褪,则验证氯气不具有漂白性,只有d符合,
故答案为:d;
(4)D、E的目的是比较氯、溴、碘的非金属性,D中发生氯气与NaBr的反应生成溴,打开活塞,将装置D中少量溶液加入装置E中,氯气、溴均可与KI反应生成碘,则E中碘易溶于苯显紫红色,出现分层后上层为紫红色的苯层,该现象不能说明溴的非金属性强于碘,过量的氯气也可将碘离子氧化,反应离子方程式Cl2+2I-=I2+2Cl-;
故答案为:E中溶液分为两层,上层(苯层)为紫红色;Cl2+2I-=I2+2Cl-;
(5)氯、溴、碘为同主族,从上到下,原子半径逐渐增大,得电子能力减弱,元素非金属性减弱;
故答案为:氯、溴、碘同主族,从上到下,原子半径逐渐增大,得电子能力减弱,元素非金属性减弱;
(6)亚硫酸钠具有强的还原性与氯气反应氧化还原反应生成硫酸钠和盐酸,反应的离子方程式:SO32-+Cl2+H2O=SO42-+2Cl-+2H+;
故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+.
点评 本题考查性质实验方案的制备,为高频考点,把握氯气的性质、制法、装置的作用及氧化还原反应原理为解答的关键,注意同主族元素性质的递变规律,题目难度中等.

 阅读快车系列答案
阅读快车系列答案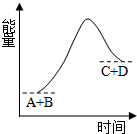
| A. | 形成C、D键释放的总能量大于断A、B键吸收的总能量 | |
| B. | 此反应反应物的总能量高于生成物的总能量 | |
| C. | 此反应为一个吸热的反应 | |
| D. | 此反应只有在加热条件下才能进行 |
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | B. | 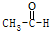 +H2$\stackrel{催化剂}{→}$CH3CH2OH +H2$\stackrel{催化剂}{→}$CH3CH2OH | ||
| C. | H2+Cl2═2HCl | D. | 2CH3CH2OH+O2→2CH3CHO+2H2O |
| A. | 分子里含有-C≡C-的不饱和链烃 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色,但原理不同 | |
| C. | 分子里所有的碳原子都在一条直线上 | |
| D. | 碳原子数相同的炔烃和二烯烃是同分异构体 |
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )?
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )?| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W? | |
| C. | 原子半径:T>Q>R | |
| D. | T的最高价氧化物对应水化物为强碱 |
| A. | 过渡元素形成的化合物 | B. | ⅢA族元素形成的化合物 | ||
| C. | ⅣA族元素形成的化合物 | D. | ⅦA族元素形成的化合物 |