题目内容
20.有A、B、C、D、E、F六种元素,已知原子序数依次增大.①E的氢化物的分子式为H2E,E的最高价氧化物中含E 40%,而且E原子核内的质子数和中子数相等;
②A原子最外层电子数是次外层电子数的2倍,B的阴离子和C、D的阳离子与氖原子的电子层结构相同,F原子的最外层电子数比次外层电子数少1;
③常温常压下,B的单质是气体,0.1摩尔B的单质与足量的氢气反应时,有2.408×1023 个电子转移;
④C的单质在B的单质中燃烧,生成淡黄色固体.此固体与AB2反应又生成B单质;
⑤0.1摩尔D单质与足量的盐酸反应,在标准状态下生成的氢气体积为3.36L.
根据上述回答:
(1)元素E位于第三周期,第ⅥA族,并画出E的离子结构示意图
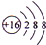 .
.(2)A、D、E、F最高价氧化物对应的水化物的化学式为H2CO3、Al(OH)3、H2SO4、HClO4.
(3)C单质在B单质中燃烧,生成物的电子式为:
 ;此固体所含化学键类型为离子键、共价键;此固体与AB2反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2.
;此固体所含化学键类型为离子键、共价键;此固体与AB2反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2.(4)证明F的非金属性大于E的非金属性(用化学方程式表示):Cl2+H2S=S↓+2HCl.
(5)写出由D的最高价氧化物的水化物制取D单质的化学反应方程式2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
分析 有A、B、C、D、E、F六种元素,已知原子序数依次增大,已知:
①E的氢化物的分子式为H2E,E的最高价氧化物的化学式为EO3,令E的相对原子质量为x,则$\frac{x}{x+48}$=40%,解得x=32,E原子的原子核中质子数和中子数相等,所以e元素原子的质子数为16,故E为硫元素;
②A原子最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故A为碳元素;B的阴离子和C、D的阳离子与氖原子的电子层结构相同,则B处于第二周期,C、D处于第三周期,F原子的最外层电子数比次外层电子数少1,结合原子序数可知,F处于第三周期,最外层电子数为7,故F为Cl元素;
③常温常压下,B的单质是气体,0.1摩尔B的单质与足量的氢气反应时,有2.408×1023 个电子转移,电子物质的量为0.4mol,结合②中B处于第二周期,可推知B为O元素;
④C的单质在B的单质中燃烧,生成淡黄色固体,则C为Na,淡黄色固体为Na2O2,Na2O2与CO2反应又生成氧气;
⑤0.1摩尔D单质与足量的盐酸反应,D为金属元素,生成氢气为$\frac{3.36L}{22.4L/mol}$=0.15mol,则反应中D的化合价为$\frac{0.15mol×2}{0.1mol}$=+3,故D为Al.
解答 解:有A、B、C、D、E、F六种元素,已知原子序数依次增大,已知:
①E的氢化物的分子式为H2E,E的最高价氧化物的化学式为EO3,令E的相对原子质量为x,则$\frac{x}{x+48}$=40%,解得x=32,E原子的原子核中质子数和中子数相等,所以e元素原子的质子数为16,故E为硫元素;
②A原子最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故A为碳元素;B的阴离子和C、D的阳离子与氖原子的电子层结构相同,则B处于第二周期,C、D处于第三周期,F原子的最外层电子数比次外层电子数少1,结合原子序数可知,F处于第三周期,最外层电子数为7,故F为Cl元素;
③常温常压下,B的单质是气体,0.1摩尔B的单质与足量的氢气反应时,有2.408×1023 个电子转移,电子物质的量为0.4mol,结合②中B处于第二周期,可推知B为O元素;
④C的单质在B的单质中燃烧,生成淡黄色固体,则C为Na,淡黄色固体为Na2O2,Na2O2与CO2反应又生成氧气;
⑤0.1摩尔D单质与足量的盐酸反应,D为金属元素,生成氢气为$\frac{3.36L}{22.4L/mol}$=0.15mol,则反应中D的化合价为$\frac{0.15mol×2}{0.1mol}$=+3,故D为Al.
(1)E为S元素,位于第三周期第ⅥA族,S2-离子结构示意图为 ,
,
故答案为:三、ⅥA; ;
;
(2)A(碳)、D(Al)、E(硫)、F(Cl)的最高价氧化物对应的水化物的化学式分别为:H2CO3、Al(OH)3、H2SO4、HClO4,
故答案为:H2CO3;Al(OH)3;H2SO4;HClO4;
(3)C单质在B单质中燃烧生成物为Na2O2,电子式为: ,含有离子键、共价键,与CO2反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2,
,含有离子键、共价键,与CO2反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2,
故答案为: ;离子键、共价键;2Na2O2+2CO2=2Na2CO3+O2;
;离子键、共价键;2Na2O2+2CO2=2Na2CO3+O2;
(4)证明F(Cl)的非金属性大于E(S)的非金属性(用化学方程式表示):Cl2+H2S=S↓+2HCl,
故答案为:Cl2+H2S=S↓+2HCl;
(5)D的最高价氧化物的水化物为Al(OH)3,由Al(OH)3制取Al单质,先加热分解得到氧化铝,再电解熔融的氧化铝冶炼Al,反应的化学反应方程式:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,
故答案为:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,是对学生综合能力的考查,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 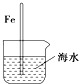 插入海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. | 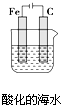 插入溶液中的铁棒容易溶解,主要是发生电化学腐蚀 | |
| C. |  燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 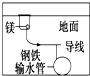 用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的阴极 |
| A. | 在1mol CaC2、KHSO4、Na2O2三种离子化合物中,所含阴、阳离子的总数均为3NA | |
| B. | 1molCu和足量热浓硫酸反应可生成nA个SO3分子 | |
| C. | 3mol单质Fe完全转变为Fe3O4,失去8nA个电子 | |
| D. | 78gNa2O2与足量水反应转移的电子数为2NA |
| A. | 标准状态下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 50mL 18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| C. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA | |
| D. | 常温常压下,14.0g乙烯与丙烯的混合物红含有氢原子的数目为2NA |
| A. | 除去铁粉中混有的少量铝粉,可加人过量的氢氧化钠溶液,完全反应后过滤 | |
| B. | 除去FeCl2溶液中少量的FeCl3,可加入过量的铁粉,完全反应后过滤 | |
| C. | 用渗析的方法可除去Fe(OH)3胶体中混有的Cl- | |
| D. | 加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3 |
2Fe2++H2O2+2H+═2Fe3++2H2O 2Fe3++H2O2═2Fe2++O2↑+2H+
下列说法正确的是( )
| A. | H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 | |
| B. | 在H2O2分解过程中,溶液的酸性增强 | |
| C. | H2O2分解的总方程式为:H2O2═H2O+O2↑ | |
| D. | H2O2生产过程要严格避免混入Fe2+ |
| A. | 对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 | |
| B. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| C. | 升高温度,一般可使活化分子的百分数增大,因而反应速率增大 | |
| D. | 加适宜的催化剂,可使活化分子的百分数大大增加,从而增大反应速率 |
