题目内容
12.温度相同、浓度均为0.2mol L-1的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤CH3COONa溶液,它们的pH值由小到大的排列顺序是( )| A. | ③①④②⑤ | B. | ①③④②⑤ | C. | ③②①④⑤ | D. | ⑤②④①③ |
分析 根据盐类水解的酸碱性和水解程度比较,①(NH4)2SO4、③NH4HSO4、④NH4NO3显酸性,、⑤CH3COONa显碱性,而②NaNO3不水解,显中性,据此分析.
解答 解:①(NH4)2SO4、④NH4NO3水解呈酸性,pH<7;③NH4HSO4电离出H+呈酸性,pH<7;②NaNO3不水解,pH=7;⑤CH3COONa水解呈碱性,pH>7,①、④比较,前者c(NH4+)大,水解生成c(H+)大,pH小,①③比较,后者电离出c(H+)比前者水解出c(H+)大,pH小,所以③①④②⑤,
故选A.
点评 本题考查溶液PH的大小比较,题目难度不大,要考虑盐类的水解程度大小,注意硫酸氢铵中硫酸氢根离子电离出氢离子.

练习册系列答案
相关题目
20.下列食物中属于酸性食物的是( )
| A. | 西红柿 | B. | 牛肉 | C. | 蜜橘 | D. | 黄瓜 |
4.300mL Al2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1mol•L-1 Ba(OH)2溶液100mL,反应后溶液中SO42-的物质的量浓度约为( )
| A. | 0.4 mol•L-1 | B. | 0.3 mol•L-1 | C. | 0.2 mol•L-1 | D. | 0.1 mol•L-1 |
2.下列物质在水溶液中,能电离出硫离子的是( )
| A. | Na2S | B. | NaHSO4 | C. | SO2 | D. | H2SO4 |
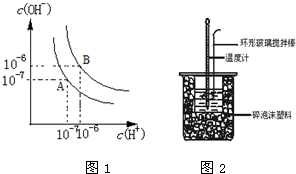 溶液的酸碱性对生产生活都有重要的影响.
溶液的酸碱性对生产生活都有重要的影响.
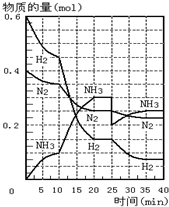 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示.则下列说法正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示.则下列说法正确的是( )