题目内容
8.玻尔理论不能解释( )| A. | H原子光谱为线状光谱 | |
| B. | 在一给定的稳定轨道上,运动的核外电子不发射能量----电磁波 | |
| C. | H原子的可见光区谱线 | |
| D. | H原子光谱的精细结构 |
分析 玻尔理论包括三条假说
1、原子能量的量子化假设:原子只能处于一系列不连续的能量状态中,在这些状态中的原子是稳定的,电子虽然做加速运动,但并不向外辐射能量;
2、原子能级的跃迁假设:原子从一个定态跃迁到另一个定态时,原子辐射一定频率的光子,光子的能量由这两种定态的能量差决定;
3、原子中电子运动轨道量子化假设:原子的不同能量状态对应于电子的不同运行轨道,由于原子的能量状态是不连续的,因此电子运动的轨道也可能是不连续的,即电子不能在任意半径的轨道上运动.
解答 解:A.原子从一个定态跃迁到另一个定态时,原子辐射一定频率的光子,光子的能量由这两种定态的能量差决定,所以H原子光谱为线状光谱,故A不选;
B.原子只能处于一系列不连续的能量状态中,在这些状态中的原子是稳定的,电子虽然做加速运动,但并不向外辐射能量,所以在一给定的稳定轨道上,运动的核外电子不发射能量,故B不选;
C.原子从一个定态跃迁到另一个定态时,原子辐射一定频率的光子,所以波尔理论能解释H原子的可见光区谱线,故C不选;
D.波尔理论本身仍是以经典理论为基础,具有一定的局限性,不能解释H原子光谱的精细结构,故D选.
故选D.
点评 本题考查了波尔理论的内容,题目难度中等,注意把握波尔理论的内容,侧重于基本原理的应用的考查.

练习册系列答案
相关题目
18.下列化合物同分异构体数目最少的是( )
| A. | 丙酸甲酯 | B. | 已烷 | C. | 已烯 | D. | 二氯丁烷 |
19.短周期元素W、X、Y的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质.根据以上叙述,下列说法中一定正确的是( )
| A. | 上述三种元素的原子半径大小为Y<X<W | |
| B. | W、X、Y原子的核外最外层电子数的总和为10 | |
| C. | 由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 | |
| D. | W与Y只能形成含极性共价键的化合物 |
16.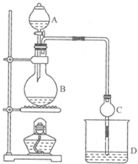 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸铵,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸铵,D中放有饱和碳酸钠溶液.
已知:①无水氯化钙可与乙醇形成难溶于水CaCl2•6C2H5OH
②有关有机物的沸点:
请回答:
(1)浓硫酸的作用:制乙酸、催化剂、脱水剂;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示
18O位置的化学方程式:CH3COOH+CH3CH218OH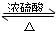 CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
(2)球形干燥管C的作用是防止倒吸、冷凝反应前向D中加入几滴酚酞,反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇;再加入(此空从下列选项中选择)C;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯:
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
(4)反应的理想温度范围在77.1-78.5℃,原因是使乙酸乙酯分离出来,防止混入杂质.因此,该装置需要改进的地方是水浴加热.
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸铵,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸铵,D中放有饱和碳酸钠溶液.已知:①无水氯化钙可与乙醇形成难溶于水CaCl2•6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用:制乙酸、催化剂、脱水剂;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示
18O位置的化学方程式:CH3COOH+CH3CH218OH
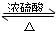 CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O(2)球形干燥管C的作用是防止倒吸、冷凝反应前向D中加入几滴酚酞,反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇;再加入(此空从下列选项中选择)C;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯:
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
(4)反应的理想温度范围在77.1-78.5℃,原因是使乙酸乙酯分离出来,防止混入杂质.因此,该装置需要改进的地方是水浴加热.
3.不能使蛋白质变性的物质是( )
(1)浓硝酸
(2)福尔马林
(3)硝酸银
(4)硫酸铵
(5)硫酸铜
(6)氢氧化钠
(7)乙醇.
(1)浓硝酸
(2)福尔马林
(3)硝酸银
(4)硫酸铵
(5)硫酸铜
(6)氢氧化钠
(7)乙醇.
| A. | (1)(2) | B. | (4)(5) | C. | (4) | D. | (4)(7) |
13.下列有关离子键的叙述中正确的是( )
| A. | 离子化合物中只含有离子键 | |
| B. | 共价化合物中可能含离子键 | |
| C. | 含离子键的化合物不一定为离子化合物 | |
| D. | 共价化合物中不含离子键 |
20.下列有关物质性质的说法中,错误的是( )
| A. | 硫是一种黄色晶体,易溶于水 | |
| B. | 新制氯水应避光保存 | |
| C. | 新制氯水具有漂白作用 | |
| D. | 二氧化氮是红棕色、有刺激性气味的有毒气体 |
17.下列关于化学键的叙述,正确的一项是( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 非金属元素组成的化合物中只含共价键 | |
| D. | 含有共价键的化合物一定是共价化合 |
18.填写下表:
| 化学反应 | 能量转化形式 |
| ①CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | 由 化学能转化为 热能 |
| ②Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O | 由 化学能转化为 电能 |
| ③CaCO3$\frac{\underline{\;高温\;}}{\;}$Ca+CO2↑ | 由 热能转化为 化学能 |
| ④6nH2O+6nCO2$→_{叶绿素}^{光}$(C6H12O6)n+6nO2 | 由 光能转化为 化学能 |