题目内容
18.下列化合物同分异构体数目最少的是( )| A. | 丙酸甲酯 | B. | 已烷 | C. | 已烯 | D. | 二氯丁烷 |
分析 A、酯类与羧酸属于同分异构体;
B、烷烃只有碳链异构;
C、烯烃存在官能团位置异构、与环烷烃互为同分异构体;
D、氯代烃存在的是官能团的位置异构,两个氯可以连在同一个碳上.
解答 解:A、丙酸甲酯的分子式为C4H8O2,其同分异构体有:乙酸乙酯、甲酸丙酯、甲酸异丙酯、正丁酸、异丁酸,还有羟基醛等多于5种;
B、己烷的同分异构体有5种;
C、己烯的同分异构体为1-己烯、2-己烯、3-己烯、2-甲基-1-戊烯、3-甲基-1-戊烯、4-甲基-1-戊烯、2-甲基-2-戊烯等多于5种;
D、二氯丁烷为丁烷中的2个H被氯原子取代生成的,丁基有4种,正丁基剩余4种H,故一氯代物有4种、异丁烷有3种H,故多于5种,据此分析最少的是己烷,故选B.
点评 本题主要考查的是同分异构体的判断,熟悉常见有机物的结构是解决本题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.A、B、C、D、E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如下图1.E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2-相同.

试回答:
(1)元素E在元素周期表中的位置是第三周期ⅣA族.
(2)与元素D离子所含电子数和质子数均相同的微粒是NH4+ (或H3O+).
(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的为H2SiO3.若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:ⅠHNO3,ⅡNa2SiO3,观察到的实验现象是中出现白色胶状沉淀.
(4)由以上五种元素组成的中学常见的物质,其组成和结构信息如下表:
①a含有的化学键有离子键、共价键;
②b与c反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.

试回答:
(1)元素E在元素周期表中的位置是第三周期ⅣA族.
(2)与元素D离子所含电子数和质子数均相同的微粒是NH4+ (或H3O+).
(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的为H2SiO3.若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:ⅠHNO3,ⅡNa2SiO3,观察到的实验现象是中出现白色胶状沉淀.
(4)由以上五种元素组成的中学常见的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A、C、D的盐 |
| b | C、D组成的化合物,且原子数之比为1:1 |
| c | 化学组成为AC2 |
②b与c反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
6.对于反应2SO2+O2$?_{加热}^{催化剂}$2SO3,下列判断正确的是( )
| A. | 2 mol SO2和足量的O2反应,可生成2 mol SO3 | |
| B. | 达到反应限度时SO2、O2、SO3的分子数之比一定为2:1:2 | |
| C. | 达到反应限度时SO2的消耗速率必定等于O2的生成速率的2倍 | |
| D. | 若反应在恒容容器中进行,气体密度保持不变,可以判定反应到达平衡 |
13.以下既是氧化还原反应,又是吸热反应的是( )
| A. | 石墨比金刚石稳定,石墨转变为金刚石的过程 | |
| B. | 氢氧化钡与氯化铵反应 | |
| C. | 碳酸钙分解 | |
| D. | 碳与水反应生成水煤气 |
10.下列关于有机物的叙述正确的是( )
| A. | 石油液化气、汽油和石蜡的主要成分都是碳氢化合物 | |
| B. | 1,2-二氯乙烷在NaOH水溶液中发生消去反应得到乙炔 | |
| C. | 由CH2=CHCOOCH3合成的聚合物为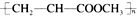 | |
| D. | 有机物中一定含有碳氢元素,可能含有氯、氧、硫等元素 |
7. 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图:下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图:下列对该化合物叙述正确的是( )
 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图:下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图:下列对该化合物叙述正确的是( )| A. | 属于芳香烃 | B. | 不能发生取代反应 | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 在一定条件下可以发生加成反应 |
8.玻尔理论不能解释( )
| A. | H原子光谱为线状光谱 | |
| B. | 在一给定的稳定轨道上,运动的核外电子不发射能量----电磁波 | |
| C. | H原子的可见光区谱线 | |
| D. | H原子光谱的精细结构 |
 .
. .
.