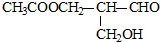题目内容
13.下列有关离子键的叙述中正确的是( )| A. | 离子化合物中只含有离子键 | |
| B. | 共价化合物中可能含离子键 | |
| C. | 含离子键的化合物不一定为离子化合物 | |
| D. | 共价化合物中不含离子键 |
分析 A、含有离子键的化合物是离子化合物,离子化合物可能含有共价键.
B、只含共价键的化合物是共价化合物.
C、离子化合物一定含有离子键.
D、只含共价键的化合物是共价化合物.
解答 解:A、离子化合物可能含有共价键,如氢氧化钠中既含离子键又含共价键,如NaOH中含有离子键和共价键,故A错误.
B、只含共价键的化合物是共价化合物,共价化合物一定不含离子键,故B错误.
C、离子化合物一定含有离子键,可能含有共价键,含离子键的化合物一定为离子化合物,故C错误.
D、只含共价键的化合物是共价化合物,所以共价化合物中一定不含离子键,故D正确.
故选D.
点评 本题考查了化合物类型和化学键类型的关系,难度不大,侧重于基础知识的考查,注意对基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.右图是元素周期表的一部分,关于图中阴影部分元素的说法中,正确的是( )
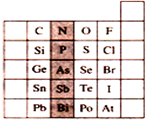

| A. | PH3的沸点比NH3高 | |
| B. | PH3的稳定性比H2S强 | |
| C. | 该纵行元素的最高价氧化物对应的水化物化学式均为H3RO4 | |
| D. | H3AsO4的酸性比H3PO4弱 |
1.丙烷的分子结构可简写成键线式结构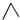 ,有机物A的键线式结构为
,有机物A的键线式结构为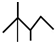 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
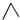 ,有机物A的键线式结构为
,有机物A的键线式结构为 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )| A. | 用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷 | |
| B. | 有机物A的一氯取代物只有4种 | |
| C. | 有机物A的分子式为C8H18 | |
| D. | B的结构可能有3种,其中一种名称为3,4,4-三甲基-2-戊烯 |
8.玻尔理论不能解释( )
| A. | H原子光谱为线状光谱 | |
| B. | 在一给定的稳定轨道上,运动的核外电子不发射能量----电磁波 | |
| C. | H原子的可见光区谱线 | |
| D. | H原子光谱的精细结构 |
18.X、Y、Z都是短周期元素,X原子的最外层只有l个电子,Y原子的M层电子数只有K层与L层电子数之和的一半,Z原子的L层电子数比Y原子的L层电子数少2,且Y元素可有2种正价,两种正价的差值为2.由X、Y、Z三种元索组成的化合物的化学式可能是( )
①X2YZ3 ②XYZ3 ③XYZ4 ④X2YZ4 ⑤X3YZ3 ⑥X3YZ4.
①X2YZ3 ②XYZ3 ③XYZ4 ④X2YZ4 ⑤X3YZ3 ⑥X3YZ4.
| A. | ①②③ | B. | ④⑤⑥ | C. | ②⑤⑥ | D. | ①③⑤ |
2.下列说法正确的是( )
| A. | 由分子组成的物质中一定存在共价键 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 非极性键只存在双原子分子中 | |
| D. | 两个非金属元素原子间不可能形成离子键 |
3.下列分子式表示的物质,有两种同分异构体的是( )
| A. | C3H8 | B. | C3H7Cl | C. | CH2Cl2 | D. | C2H6O |