题目内容
18.已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3H2O+3Cu,用下图所示装置可以实现该反应,A中加的是氯化铵和氢氧化钙固体,C中的固体是氧化铜.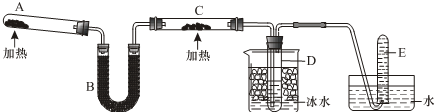
回答下列问题:
(1)A中发生反应的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.
(2)B中加入的物质是碱石灰.
(3)实验时在C中观察到的现象是黑色固体逐渐变成红色,该反应中氨的作用是还原剂(填氧化剂或还原剂).
(4)检验实验后试管D中物质的方法和现象是用红色石蕊试纸检验,试纸变蓝,用无水硫酸铜检验,无水硫酸铜变蓝.
分析 (1)氯化铵与氢氧化钙反应生成氯化钙、氨气和水;
(2)A中制取的氨气中含有水蒸气,应进行干燥,氨气为碱性气体,应选择碱性干燥剂;
(3)氨气与氧化铜发生氧化还原反应,氧化铜被还原生成铜;依据氨气与铜的反应中氨气中元素化合价变化判断氨气的作用;
(4)氨气还原氧化铜之后剩余的氨气和产生的水蒸气在冷凝时会形成氨水,具有氨气分子和结晶水的成分,氨水可以使使红色石蕊试纸变蓝,其中的结晶水会使无水硫酸铜变蓝.
解答 解:(1)氯化铵与氢氧化钙反应生成氯化钙、氨气和水,化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O;
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O;
(2)B中物质为碱石灰,用来干燥氨气;
故答案为:碱石灰;
(3)根据2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3H2O+3Cu知,C中黑色固体CuO变为红色Cu,所以看到的现象是黑色固体逐渐变成红色,氨气在反应中N元素化合价升高被氧化,做还原剂;
故答案为:黑色固体逐渐变成红色;还原剂;
(4)氨气还原氧化铜之后剩余的氨气和产生的水蒸气在冷凝时会形成氨水,具有氨气分子和结晶水的成分,氨水可以使使红色石蕊试纸变蓝,其中的结晶水会使无水硫酸铜变蓝,所以检验检验该物质的方法是:用红色石蕊试纸检验,试纸变蓝,用无水硫酸铜检验,无水硫酸铜变蓝;
故答案为:用红色石蕊试纸检验,试纸变蓝,用无水硫酸铜检验,无水硫酸铜变蓝.
点评 本题考查了氨气的制备和性质的检验,熟悉氨气制备原理是解题关键,题目难度不大.

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案| A. | 7 g | B. | 14 g | C. | 28 g | D. | 无法计算 |
| A. | 硫在氧气中燃烧 | B. | 硫化氢在氧气中燃烧 | ||
| C. | 铁粉与硫粉混合加热 | D. | 铜在空气中加热 |
| A. | 反应所生成的气体体积:a杯>b杯 | B. | 反应所需要的时间:a杯>b杯 | ||
| C. | 刚开始时反应的速率:b杯>a杯 | D. | 整个反应阶段平均速率:a杯>b杯 |
| A. | C02与CaO化合是放热反应,则CaC03分解是吸热反应 | |
| B. | 只有分解反应才是吸热反应 | |
| C. | 使用催化剂的反应是吸热反应 | |
| D. | 凡需加热的反应一定是吸热反应 |
 、C:CH3CH2OH D:CH3COOH
、C:CH3CH2OH D:CH3COOH 在FeBr3催化作用下,与液溴反应的化学方程式为:
在FeBr3催化作用下,与液溴反应的化学方程式为: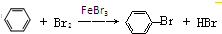 .
.