题目内容
13.关于右边一组图示的说法中错误的是( )| A. |  用图实验可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. |  用图实验可用于比较铝、铁的金属性的强弱 | |
| C. |  图表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为吸热反应 | |
| D. | 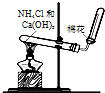 图装置可用于实验室制取氨气 |
分析 A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
B.较活泼金属能置换出较不活泼金属;
C.反应物总能量大于生成物总能量,则该反应是放热反应,否则是吸热反应;
D.实验室用氢氧化钙和氯化铵加热制取氨气,氨气密度小于空气,且常温下和空气不反应,可以采用向下排空气法收集.
解答 解:A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,稀硫酸和碳酸钠反应生成二氧化碳,二氧化碳、水和硅酸钠反应生成难溶性的硅酸,且这几种酸分别是其最高价氧化物的水化物,所以可以实现实验目的,故A正确;
B.较活泼金属能置换出较不活泼金属,铝能和氧化铁发生铝热反应生成Fe,说明金属性Al>Fe,故B正确;
C.反应物总能量大于生成物总能量,则该反应是放热反应,否则是吸热反应,根据图知,反应物总能量大于生成物总能量,所以该反应是放热反应,故C错误;
D.实验室用氢氧化钙和氯化铵加热制取氨气,氨气密度小于空气,且常温下和空气不反应,可以采用向下排空气法收集,所以实验装置符合氨气的制备,故D正确;
故选C.
点评 本题考查化学实验评价及反应热的判断,为高频考点,明确实验原理及物质性质是解本题关键,注意从实验原理方面分析评价,如果将A中的稀硫酸换为稀盐酸就不能证明非金属性强弱,因为HCl不是Cl元素的最高价氧化物的水化物,且盐酸易挥发而干扰实验,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
3.表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)上述元素中,化学性质最不活泼的是Ar(填元素符号).
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4(填元素符号).
(3)元素②的气态氢化物分子属于非电解质(填电解质或非电解质);元素⑦与④形成化合物的电子式是 .
.
(4)元素⑤的最高价氧化物与氢氧化钠溶液反应的离子方程式为:Al2O3+2OH-=H2O+2AlO2-.
(5)元素④的某氧化物可作供氧剂,该氧化物中所含的化学键类型有离子键、共价键,写出其与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 零 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4(填元素符号).
(3)元素②的气态氢化物分子属于非电解质(填电解质或非电解质);元素⑦与④形成化合物的电子式是
 .
.(4)元素⑤的最高价氧化物与氢氧化钠溶液反应的离子方程式为:Al2O3+2OH-=H2O+2AlO2-.
(5)元素④的某氧化物可作供氧剂,该氧化物中所含的化学键类型有离子键、共价键,写出其与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
4.用NA表示阿伏加德罗常数的数值.下列叙述中正确的是( )
| A. | 1molC2H6O中含有C-C键的数目一定为NA | |
| B. | 25℃,pH=12的NaHCO3溶液中含有OH-的数目为0.01NA | |
| C. | 标准状况下,2.24L异丁烷含有的分子数目为0.1NA | |
| D. | 常温常压下,0.3molNO2与足量H2O充分反应,转移电子的数目为0.3NA |
1.已知常温下:KSP(AgCl)=1.8×10-10mol2•L-2,KSP(Ag2CrO4)=1.9×10-12mol3•L-3则常温时下列叙述正确的是( )
| A. | AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小 | |
| B. | KSP(AgCl)>KSP(Ag2CrO4),可说明Ag2CrO4比AgCl难溶于水 | |
| C. | 将0.00lmol•L-1AgNO3溶液滴入0.001 mol•L-1KC1和0.00lmol•L-1K2CrO4混合溶液中,先产生Ag2CrO4沉淀 | |
| D. | 同AgCl的悬浊液中滴加浓氨水后沉淀溶解,是因为生成了银氨离子而使AgCl的溶解平衡向右移动 |
5.下列说法正确的是( )
| A. | 22.4LO2中一定含有6.02×1023个氧分子 | |
| B. | 将8.0gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为0.2mol/L | |
| C. | 阿伏加德罗常数个H2O分子在标准状况下的体积是22.4L | |
| D. | 在标准状况下,20mLNH3与60mLO2所含的分子个数比为1:3 |
3.用下列装置进行相应的实验,能达到实验目的是( )


| A. | 用图1装置制取乙酸乙酯 | |
| B. | 用图2装置制取、收集乙炔气体 | |
| C. | 用图3检验溴乙烷与NaOH的醇溶液共热产生的乙烯 | |
| D. | 用图4检验C2H5OH 与浓H2SO4加热至170℃制取乙烯 |
 一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu═2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-═Cu2+,还原反应式:2Fe3++2e-═2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu═2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-═Cu2+,还原反应式:2Fe3++2e-═2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题: A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示:
A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示: CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O .
.