题目内容
4.用NA表示阿伏加德罗常数的数值.下列叙述中正确的是( )| A. | 1molC2H6O中含有C-C键的数目一定为NA | |
| B. | 25℃,pH=12的NaHCO3溶液中含有OH-的数目为0.01NA | |
| C. | 标准状况下,2.24L异丁烷含有的分子数目为0.1NA | |
| D. | 常温常压下,0.3molNO2与足量H2O充分反应,转移电子的数目为0.3NA |
分析 A、C2H6O的结构可能为CH3CH2OH,也可能为CH3OCH3;
B、溶液体积不明确;
C、求出异丁烷的物质的量,然后根据分子数目N=nNA来计算;
D、NO2与足量H2O反应是歧化反应.
解答 解:A、C2H6O的结构可能为CH3CH2OH,也可能为CH3OCH3,当为乙醇时,1molC2H6O含1molC-C键,当为二甲醚时,1molC2H6O不含C-C键,故A错误;
B、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故B错误;
C、标况下,2.24L异丁烷的物质的量为0.1mol,故分子数目N=nNA=0.1NA个,故C正确;
D、NO2与足量H2O反应是歧化反应,3molNO2转移2mol电子,则0.3molNO2与足量H2O充分反应,转移电子的数目为0.2NA,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.下列叙述中正确的是( )
| A. | P4和NO2都是共价化合物 | |
| B. | 在CaO和SiO2晶体中,都不存在单个小分子 | |
| C. | CCl4和NH3都是以极性键结合的极性分子 | |
| D. | 甲烷是对称的平面结构,所以是非极性分子 |
12.下列说法正确的是( )
| A. | 盐酸、氨气和碳酸钠都是电解质 | |
| B. | 常温常压下,22.4L CO2气体的物质的量大于1mol | |
| C. | 2.4克石墨和C60的混合物所含碳原子数约为0.2×6.02×1023 | |
| D. | 氢氧化铁胶体较稳定,是因为该胶体带有正电荷 |
19.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | NH3的结构式为: | ||
| C. | CH4 分子的比例模型: | D. | -CH3(甲基)的电子式为: |
9.在一定体积和一定条件下有反应N2+3H2?2NH3,现分别从两条途径建立平衡:
Ⅰ.起始浓度 N2:l mol•L -1,H2:3mol•L -1
Ⅱ.起始浓度 N2:2mol•L -1,H2:6mol•L -1
则下列叙述正确的是( )
Ⅰ.起始浓度 N2:l mol•L -1,H2:3mol•L -1
Ⅱ.起始浓度 N2:2mol•L -1,H2:6mol•L -1
则下列叙述正确的是( )
| A. | Ⅰ和II两途径达到平衡时,体系内各成分的体积分数相同 | |
| B. | 达到平衡时,Ⅰ途径的反应速率v(H2)等于Ⅱ途径的反应速率v(H2) | |
| C. | 达到平衡时,Ⅱ途径体系内混合气体的压强是Ⅰ途径内混合气体压强的2倍 | |
| D. | 达到平衡时,Ⅰ途径体系内混合气体的密度为途径Ⅱ体系内混合气体的密度的$\frac{1}{2}$ |
16.用下列装置不能达到有关实验目的是( )
| A. |  用图装置电解精炼铝 用图装置电解精炼铝 | |
| B. |  用图装置制备Fe(OH)2 用图装置制备Fe(OH)2 | |
| C. |  用图装置可制得金属锰 用图装置可制得金属锰 | |
| D. |  用图装置验证NaHCO3和Na2CO3的热稳定性 用图装置验证NaHCO3和Na2CO3的热稳定性 |
13.关于右边一组图示的说法中错误的是( )
| A. |  用图实验可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. |  用图实验可用于比较铝、铁的金属性的强弱 | |
| C. |  图表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为吸热反应 | |
| D. | 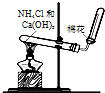 图装置可用于实验室制取氨气 |
