题目内容
12.请从图中选用必要的装置进行电解饱和食盐水的实验,要求制定产生的氢气的条件(大于25ML),并检验氯气的氧化性.(1)A极发生的电极反应式是2H++2e-=H2↑,B极发生的电极反应式是2Cl--2e-=Cl2↑.
(2)设计上述气体实验装置时,各接口的正确连接顺序为:H接F、G接A、B接D、E接C;
(3)在实验中,盛有KI淀粉溶液的容器中发生反应的离子方程式为Cl2+2I-=I2+2Cl-.

分析 (1)A是阴极、B是阳极,用惰性电极电解饱和食盐水时,阴极上氢离子放电生成氢气,阳极上氯离子放电生成氯气;
(2)氯气具有强氧化性,能氧化碘离子生成碘,碘遇淀粉试液变蓝色,所以可以用淀粉KI溶液检验氯气的氧化性,氯气有毒不能排空,应该用碱液吸收尾气;氢气不易溶于水,可以采用排水法收集氢气;
(3)氯气和碘离子发生置换反应生成碘和氯离子.
解答 解:(1)A是阴极、B是阳极,用惰性电极电解饱和食盐水时,阴极上氢离子放电生成氢气,阳极上氯离子放电生成氯气,所以阴极、阳极电极反应式分别为2H++2e-=H2↑、2Cl--2e-=Cl2↑,故答案为:2H++2e-=H2↑;2Cl--2e-=Cl2↑;
(2)氯气具有强氧化性,能氧化碘离子生成碘,碘遇淀粉试液变蓝色,所以可以用淀粉KI溶液检验氯气的氧化性,氯气有毒不能排空,应该用碱液吸收尾气;氢气不易溶于水,可以采用排水法收集氢气,所以仪器连接顺序是A接G、F接H;B接D、E接C,
故答案为:H;F;G;D;E;C;
(3)氯气和碘离子发生置换反应生成碘和氯离子,离子方程式为Cl2+2I-=I2+2Cl-,故答案为:Cl2+2I-=I2+2Cl-.
点评 本题以电解原理为载体考查实验基本操作及物质性质,明确实验目的是解本题关键,根据实验目的及物质性质选取合适的实验装置及连接顺序,难点是实验仪器的连接顺序,题目难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
2.如图,表示正反应是吸热的是( )
| A. | 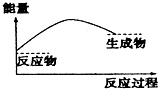 | B. |  | ||
| C. | 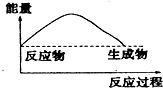 | D. |  |
3.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.
(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为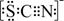 .
.
①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
③通过实验证明了SCN-中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成.
④若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
| 操 作 | 现 象 |
通入氯气至过量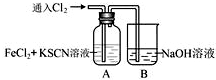 | I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
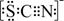 .
.①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
③通过实验证明了SCN-中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成.
④若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
20.室温下,下列有关两种溶液的说法不正确的是( )
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A. | ①②两溶液中c(OH-)相等 | |
| B. | ①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>② | |
| C. | ①溶液的物质的量浓度为0.01mol•L-1 | |
| D. | 等体积的①②两溶液分别与0.01 mol•L-1的盐酸完全中和,消耗盐酸的体积:①>② |
7.核电荷数为16的元素和核电荷数为4的原子相比较,前者的下列数据是后者的4倍的是( )
| A. | 原子半径 | B. | 最外层电子数 | C. | 电子层数 | D. | 次外层电子数 |
17.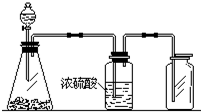 如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )
如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )
 如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )
如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )| A. | 制取NO气体 | B. | 制取二氧化碳气体 | ||
| C. | 制取氯气 | D. | 制取氨气 |
4.X+、Y2+、Z3+、W2-均为第三周期元索的简单离子,其中不影响水的电离平衡的微粒是( )
| A. | X+ | B. | Y2+ | C. | Z3+ | D. | W2- |
1.如图.4种短周期元索W、X、Y、Z,它们原子的最外层电子数之和为22.下列说法正确的是(
| X | Y | ||
| W | Z | ||
| T |
| A. | X、Y、Z最低价氢化物的沸点依次升高 | |
| B. | X、Y和氢形成的化合物中只有共价键 | |
| C. | WY2、W3X4、WZ4均为原子晶体 | |
| D. | 元素T的单质可作半导体材料,T与Z元素可形成化合物TZ4 |
2.下列有关σ键的说法错误的是( )
| A. | 如果电子云图象是由两个s电子重叠形成的,即形成s-sσ键 | |
| B. | s电子与p电子形成s-pσ键 | |
| C. | p电子和p电子不能形成σ键 | |
| D. | HCl分子里含有一个s-pσ键 |