题目内容
7.核电荷数为16的元素和核电荷数为4的原子相比较,前者的下列数据是后者的4倍的是( )| A. | 原子半径 | B. | 最外层电子数 | C. | 电子层数 | D. | 次外层电子数 |
分析 16号元素和4号元素的原子的结构示意图分别为: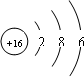 、
、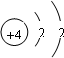 ,原子的原子序数=核外电子数=核内质子数,然后根据原子结构示意图判断选项.
,原子的原子序数=核外电子数=核内质子数,然后根据原子结构示意图判断选项.
解答 解:因16号元素和4号元素的原子的结构示意图分别为: 、
、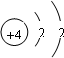 ,原子的原子序数=核外电子数=核内质子数,则
,原子的原子序数=核外电子数=核内质子数,则
A、原子半径16号元素比4号元素大,但不能确定是4倍,故A错误;
B、最外层电子数是3倍,故B错误;
C、电子层数是1.5倍,故C错误;
D、次外层电子数是4倍,故D正确;
故选D.
点评 本题考查的是核外电子判断,难度不大,能画出核外电子排布图是解本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.短周期元素Q、R、T、W在元素周期表中的位置如表所示,其中T所处的周期序数与族序数相等,请回答下列问题:
(1)T的原子结构示意图为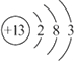 .
.
(2)元素的原子的得电子能力为:Q<W(填“>”或“<”).
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是具有漂白性的气体,反应的化学方程式为:S+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$3SO2↑+2H2O.
| Q | R | ||
| T | W |
 .
.(2)元素的原子的得电子能力为:Q<W(填“>”或“<”).
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是具有漂白性的气体,反应的化学方程式为:S+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$3SO2↑+2H2O.
15.下列离子方程式书写正确的是( )
| A. | 碳酸氢钠的水解反应:HCO3-+OH-?CO32-+H2O | |
| B. | 向澄清石灰水中加入盐酸:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | Cl2通入热的KOH溶液中制取KClO3:3Cl2+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$ClO3-+5Cl-+3H2O | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO32- |
2.分子式为C6H12O2并能与饱和碳酸氢钠溶液反应放出气体的有机物有(不含立体异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
19.下列说法不正确的是( )
| A. | 向含硫燃煤中添加适量CaO可以减少SO2的排放 | |
| B. | 工业氨氧化法制HNO3,每一步都涉及氧化还原反应 | |
| C. | 用Ba(NO3)2溶液鉴别SO32-和SO42- | |
| D. | 往铜粉理逐滴加入稀盐酸,再加入NaNO3溶液后,溶液颜色无变化 |
16.用丙醛制取1,2-丙二醇,其合成路线依次发生的反应类型为( )
| A. | 还原→取代→加成→消去 | B. | 氧化→加成→取代→消去 | ||
| C. | 消去→加聚→取代→还原 | D. | 还原→消去→加成→取代 |
17.下列说法正确的是( )
| A. | 最外层有2个电子的元素都是金属元素 | |
| B. | 不管哪一个电子层作为最外层,其电子数都不能超过8个 | |
| C. | 在原子核外的电子层中,电子层大的能量低,电子层小的能量高 | |
| D. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
