题目内容
6.工业废水中常含有一定量的Cr2O72-和CrO42-,它们对人类及生态系统产生很大损害,必须进行处理后方可排放.常用的处理方法有两种.方法1:还原沉淀法.该法的工艺流程为:ClO${\;}_{4}^{2-}$$→_{①转化}^{H+}$Cl2O${\;}_{3}^{2-}$$→_{②还原}^{Fe_{2}+}$Cl3+$→_{③沉淀}^{OH-}$Cl(OH)3↓,其中第①步存在平衡:2CrO42- (黄色)+2H+?Cr2O72- (橙色)+H2O
(1)若第①步中平衡体系的pH=2,则该溶液显橙色;向该溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡向左移动(填“向左”或“向右”或“不变”),溶液颜色将变浅.
(2)能说明第①步反应达平衡状态的是C(选填编号)
A.Cr2O72-和CrO42-的浓度相同
B.2v(Cr2O72-)=v(CrO42-)
C.溶液的颜色不变
(3)若改变条件使平衡状态的第①步反应向正反应方向移动,则该反应AB(选填编号)
A.平衡常数K值可以不改变
B.再达平衡前正反应速率一定大于逆反应速率
C.Cr2O72-的浓度一定增大
D.平衡移动时正反应速率一定先增大后减小
(4)第②步中,还原1mol Cr2O72-离子,需要6mol的FeSO4•7H2O.
(5)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)?Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至5.
方法2:电解法.该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解的进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(6)①用Fe做电极的原因为阳极反应为Fe-2e-=Fe2+,提供还原剂Fe2+.
②在阴极附近溶液pH升高的原因是(用电极反应解释)2H++2e-=H2↑,溶液中同时生成的沉淀还有Fe(OH)3.
分析 (1)根据外界条件对平衡的影响来确定平衡移动方向,从而确定离子浓度大小和溶液颜色变化;
(2)根据判断平衡状态的方法:V正=V逆,或各组分的浓度保持不变则说明已达平衡,也可根据化学平衡状态的特征:逆、定、动、变、等来回答判断;
(3)根据影响化学反应速率和化学平衡移动的因素来回答判断即可;
(4)在氧化还原反应中,化合价升高值=化合价降低值=转移电子数来计算;
(5)根据Ksp=c(Cr3+)•c3(OH-)来计算氢氧根离子离子的浓度,并计算氢离子浓度和pH的大小;
(6)①阳极是活性电极时,阳极本身失电子,生成阳离子;
②溶液PH升高的原因是溶液中氢离子浓度减少,即氢离子在阴极得电子,PH升高,氢氧根离子浓度增大,离子浓度幂的乘积大于溶度积,所以金属阳离子会生成氢氧化物沉淀.
解答 解:(1)c(H+)增大,平衡2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O右移,溶液呈橙色,向该溶液中加入Ba(NO3)2溶液,沉淀CrO42- 转化成BaCrO4沉淀,所以平衡向左移动,溶液颜色变浅;
故答案为:橙;向左;变浅;
(2)对于平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O,
A.Cr2O72-和CrO42-的浓度相同,不一定平衡,故A错误;
B.2υ(Cr2O72-)=υ(CrO42-)不能证明正逆速率相等,所以不是平衡状态,故B错误;
C.溶液的颜色不变,即有色离子浓度不会再不变,达到了化学平衡状态,故C正确;
故选C;
(3)对于平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O
A.若是浓度引起的平衡的移动,则平衡常数K值可以不改变,故A正确;
B.只要是化学平衡正向移动,则正反应速率一定大于逆反应速率,故B正确;
C.加水稀释,平衡正向移动,但是Cr2O72-的浓度一定减小,故C错误;
D.只要是化学平衡正向移动,正反应速率大于逆反应速率,但是可以增大还可以减小,故D错误.
故选AB.
(4)还原1mol Cr2O72-离子,铬元素化合价从+6价降低到+3价,一共得到电子6mol,亚铁离子被氧化为+3价,应该得到6mol电子,所以还原1mol Cr2O72-离子,
需要6mol的FeSO4•7H2O,故答案为:6;
(5)Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,则需c(OH-)=$\root{3}{\frac{Ksp}{c(Cr{\;}^{3+})}}$=$\root{3}{\frac{10{\;}^{-32}}{10{\;}^{-5}}}$=10-9mol/L,所以c(H+)=10-5mol/L,即pH=5,故答案为:5.
(6)①在电解法除铬中,铁作阳极,阳极反应为Fe-2e-═Fe2+,以提供还原剂Fe2+,
故答案为:阳极反应为Fe-2e-=Fe2+,提供还原剂Fe2+;
②在阴极附近溶液pH升高的原因是水电离产生的H+放电生成H2:2H++2e-═H2↑;同时大量产生了OH-,所以溶液中的Fe3+也将转化为Fe(OH)3沉淀;
故答案为:2H++2e-=H2↑;Fe(OH)3.
点评 本题主要考查了铬及其化合物的性质、氧化还原反应、沉淀溶解平衡和电化学知识等内容,难度中等,抓住题目信息是解题的关键.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案| A. | 乙醇完全燃烧生成水 | |
| B. | 乙醇容易挥发 | |
| C. | 乙醇能与水以任意比例互溶 | |
| D. | 0.1mol乙醇与足量金属钠反应生成0.05molH2 |
| A. |  的分子式为C17H24O3 的分子式为C17H24O3 | |
| B. | 结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物,其单体是乙炔 | |
| C. | 有机硅聚醚(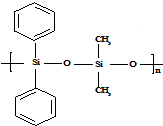 )可由单体 )可由单体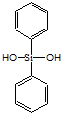 和 和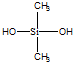 缩聚而成 缩聚而成 | |
| D. | 等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增 |
| A. | CaC2含C≡C键 | B. | Mg3C2含C-C键 | C. | As4S4含As-As键 | D. | S8含S=S键 |
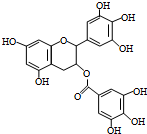 绿茶中含有的EGCG具有抗癌作用,能使白血病中的癌细胞发生自杀性死亡.已知EGCG的结构简式如图,下列有关说法错误的是( )
绿茶中含有的EGCG具有抗癌作用,能使白血病中的癌细胞发生自杀性死亡.已知EGCG的结构简式如图,下列有关说法错误的是( )| A. | EGCG的分子式为C22H18O11 | |
| B. | 1mol EGCG最多可与含9mol NaOH的溶液反应 | |
| C. | EGCG在空气中易被氧化,不能与溴水发生加成反应 | |
| D. | EGCG不能与Na2CO3溶液反应 |
| A. | 标准状况下,11.2L的正戊烷所含的分子数为0.5NA | |
| B. | 1 mol甲基中的电子数目为9NA | |
| C. | 28g乙烯所含共用电子对数目为4NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为NA |




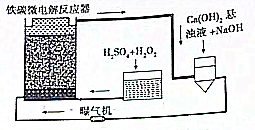 铁碳微电解技术是近年来处理各种污水的一种重要方法,其装置如图所示.
铁碳微电解技术是近年来处理各种污水的一种重要方法,其装置如图所示.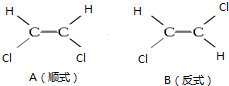 1,2一二氯乙烯有如图两种结构.
1,2一二氯乙烯有如图两种结构.