题目内容
9.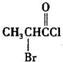 、
、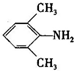 是合成施安卡因(
是合成施安卡因(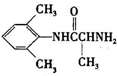 ,一种抗心律失学药物)的中间体,分别由如图所示路线合成:
,一种抗心律失学药物)的中间体,分别由如图所示路线合成: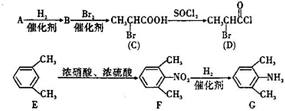 ,已知氨基(-NH2)、亚氨基(-NH-)均有碱性.
,已知氨基(-NH2)、亚氨基(-NH-)均有碱性.(1)A的分子式为C3H4O2,则A中所含官能团的名称是羧基、碳碳双键.
(2)C→D的反应类型是取代反应,F→G的反应类型是还原反应.
(3)C的系统命名法命名为2-溴丙酸,C与足量NaOH醇溶液共热时反应的化学方程式为
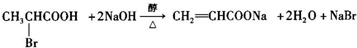 ;
;(4)E→F的化学方程式为
 ;
;(5)写出符合下列条件的F的同分异构体的结构简式
 ;
;①分子中苯环上有2种不同类型的氢原子.
②具有两性.
③与碳酸氢钠溶液反应生产二氧化碳气体.
分析 (1)A的分子式为C3H4O2,与氢气反应生成B,B与溴反应生成CH3CHBrCOOH,逆推可推知B为CH3CH2COOH,A为CH2=CHCOOH;
(2)对比C、D的结构可知,CH3CHBrCOOH中羧基上的-OH被-Cl取代生成D;对比F、G的结构可知,E中硝基转化为氨基得到G;
(3)以羧酸为母体,Br原子处于2号碳原子;C中含有溴原子、羧基,在氢氧化钠醇溶液、加热条件下发生消去反应、中和反应;
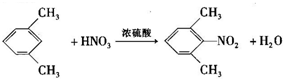
(4)E→F是硝基取代苯环上氢原子生成F;
(5)F的同分异构体满足:②具有两性,可能为氨基酸;③与碳酸氢钠溶液反应生产二氧化碳气体,含有羧基,①分子中苯环上有2种不同类型的氢原子,说明分子为对称结构,应为含有2个不同的取代基,且处于对位.
解答 解:(1)A的分子式为C3H4O2,与氢气反应生成B,B与溴反应生成CH3CHBrCOOH,逆推可推知B为CH3CH2COOH,A为CH2=CHCOOH,含有官能团为:羧基、碳碳双键,
故答案为:羧基、碳碳双键;
(2)对比C、D的结构可知,CH3CHBrCOOH中羧基上的-OH被-Cl取代生成D,属于取代反应;
对比F、G的结构可知,E中硝基转化为氨基得到G,属于还原反应,
故答案为:取代反应;还原反应;
(3)以羧酸为母体,Br原子处于2号碳原子,C的名称为:2-溴丙酸;C中含有溴原子、羧基,在氢氧化钠醇溶液、加热条件下发生消去反应、中和反应,反应方程式为: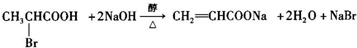 ,
,
故答案为:2-溴丙酸;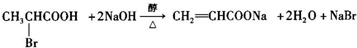 ;
;
(4)E→F是硝基取代苯环上氢原子生成F,反应方程式为: ,
,
故答案为: ;
;
(5)F的同分异构体满足:②具有两性,可能为氨基酸;③与碳酸氢钠溶液反应生产二氧化碳气体,含有羧基,①分子中苯环上有2种不同类型的氢原子,说明分子为对称结构,应为含有2个不同的取代基,且处于对位,符合条件的同分异构体有: ,
,
故答案为: .
.
点评 本题考查有机物推断与合成、官能团结构与性质、限制条件同分异构体书写等,注意根据有机物的进行分析解答,侧重考查学生分析推理能力、知识迁移应用能力,(3)中方程式书写为易错点,学生容易忽略中和反应,难度中等.

| 选项 | 实验目的 | 操作 |
| A | 从溴水中提取单质溴 | 先用CCl4 萃取分液后,再蒸馏 |
| B | 证明 Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2mL1mol•L-1NaOH溶液中先加入3滴1mol•L-1MgCl2溶液,再加入3滴1mol•L-1FeCl3 溶液 |
| C | 验证蔗糖是否水解生成葡萄糖 | 向蔗糖溶液中加入少量稀硫酸加热,再加入少量NaOH溶液,调至碱性,然后加银氨溶液水浴加热 |
| D | 证明碱的非金属性强于硅 | 向NaSiO3溶液中通入适量CO2 气体,有白色胶状沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
| A. | CH3CH2CH2CH3 | B. | CH3-CH=CHCH3 | C. | HC≡C-CH2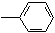 | D. | CH3-C≡C-C≡C-CH3 |
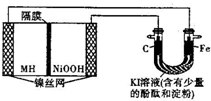 如图中的左侧装置是一种金属氢化物镍电池,其中的MH是吸附了氢原子的储氢合金,电解质溶液KOH.右侧装置是一电解池,电极材料及电解质溶液如图所示,下列有关此实验的叙述中,正确的是( )
如图中的左侧装置是一种金属氢化物镍电池,其中的MH是吸附了氢原子的储氢合金,电解质溶液KOH.右侧装置是一电解池,电极材料及电解质溶液如图所示,下列有关此实验的叙述中,正确的是( )| A. | 放电时负极反应为:MH+OH-=M+H2O+e- | |
| B. | 充电时隔膜旁的OH-从右向左移动 | |
| C. | 右侧装置中的铁电极附近溶液呈蓝色 | |
| D. | 右侧装置中的碳电极表面逸出无色、无味的气体 |
| A. | 其它条件不变,增大压强,平衡不发生移动 | |
| B. | 该反应式中n值一定为2 | |
| C. | 其它条件不变,增大压强,混合气体的总质量不变 | |
| D. | 原混合气中A与B的物质的量之比为2:1,且2M(A)+M(B)=3M(D)(其中M表示物质的摩尔质量) |
 利用下列反应:Fe+2Fe3+═3Fe2+,设计一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选):①画出实验装置图;②注明正负极材料和电解质溶液;③标出电子流动方向.
利用下列反应:Fe+2Fe3+═3Fe2+,设计一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选):①画出实验装置图;②注明正负极材料和电解质溶液;③标出电子流动方向. Ⅰ.第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要.天然气水合物是种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O他子.根据上述信息,完成下面两题:
Ⅰ.第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要.天然气水合物是种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O他子.根据上述信息,完成下面两题: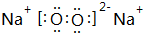 ;
; 碳元素是构成有机物的基础元素.
碳元素是构成有机物的基础元素.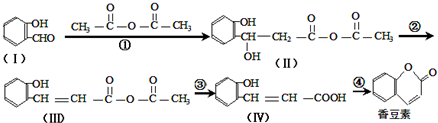
 .
. .
.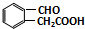 或
或 (任写一种).
(任写一种).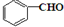 与CH3CHO两者之间能发生类似①、②的两步反应,则生成有机物的结构简式为
与CH3CHO两者之间能发生类似①、②的两步反应,则生成有机物的结构简式为 .
.