题目内容
13.设nA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 0.1 mol•L-1Ba(OH)2溶液中含有0.2nA个OH- | |
| B. | 1mol Na与足量水反应,转移2nA个电子 | |
| C. | 常温常压下,22.4L乙烯含有nA个CH2=CH2分子 | |
| D. | 常温常压下,46g NO2含有2nA个氧原子 |
分析 A、溶液体积不明确;
B、根据反应后钠元素的化合价来分析;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、求出二氧化氮的物质的量,然后根据1mol二氧化氮中含2mol氧原子来分析.
解答 解:A、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故A错误;
B、反应后钠元素的化合价为+1价,故1mol钠转移1mol电子,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L乙烯的物质的量小于1mol,故含有的乙烯分子个数小于nA个,故C错误;
D、46g二氧化氮的物质的量为1mol,而1mol二氧化氮中含2mol氧原子,即2nA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.当大量氯气泄漏时,用浸润下列某物质水溶液的毛巾捂住鼻子可防中毒.适宜的物质是( )
| A. | NaOH | B. | KI | C. | NH3 | D. | Na2CO3 |
8.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24LCCl4中含Cl原子数目为0.4NA | |
| B. | 白磷分子(P4)呈正四面体结构,12.4 g白磷中含有P-P键数目为0.6NA | |
| C. | 5.6 g铁粉在2.24l(标准状况)氯气中充分燃烧,失去的电子数为0.3NA | |
| D. | 常温常压下,10 g46%酒精水溶液中含氧原子总数为0.1NA |
18.下列微粒可以大量共存于同一溶液中的是( )
| A. | NH4+、CH3COO-、Ca2+、Cl- | B. | Fe3+、Ag+、SO42-、NO3- | ||
| C. | Cu2+、H+、S2-、NO3- | D. | C6H5OH、Fe3+、K+、Cl- |
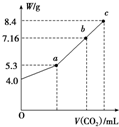 钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化.完成下列计算:
钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化.完成下列计算:
 ,该氢化物中含有的化学键是极性共价键.
,该氢化物中含有的化学键是极性共价键.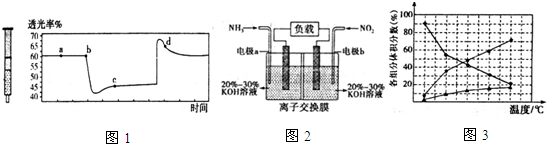
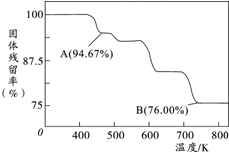 铬元素及其化合物在生产、生活中具有广泛的用途.
铬元素及其化合物在生产、生活中具有广泛的用途.