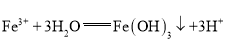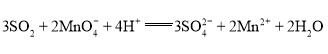题目内容
【题目】I.《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)l0Be和9Be_____________(填序号)。
a.是同一种原子 b.具有相同的中子数 c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:_________________________。
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是____________(填序号)。
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
II.下表列出了①~⑩10种元素在周期表中的位置。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑤ | ⑥ | ⑩ | |||||
3 | ① | ③ | ④ | ⑦ | ⑧ | |||
4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)________,③④⑤三种元素的原子半径由大到小的顺序是____________。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________(填化学式)
(3)元素⑥的氢化物的电子式为____________,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为_______________________________________。
【答案】cd A1(OH)3+NaOH= NaAlO2+2H2O ac K Mg>Al>C HClO4 ![]() NH3+HNO3=NH4NO3
NH3+HNO3=NH4NO3
【解析】
I(1)a.l0Be和9Be是同一元素的两种不同种原子,a错误;
b.根据质量数A=质子数Z+中子数N可知,l0Be和9Be具有的中子数分别为6和5,b错误;
c.l0Be和9Be在周期表中的位置相同,故具有相同的化学性质,c正确;
d.l0Be和9Be是具有相同质子数而不同中子数的同一元素的不同原子,故互为同位素,d正确;
故答案为:cd;
(2)A1(OH)3与NaOH溶液反应生成可溶性的NaAlO2和H2O,其化学方程式为:A1(OH)3+NaOH= NaAlO2+2H2O,故答案为:A1(OH)3+NaOH= NaAlO2+2H2O;
(3)a.Mg(OH)2与A1(OH)3分别是Mg和Al的最高价氧化物对应水化物,比较Mg(OH)2与A1(OH)3的碱性强弱来比较Mg和Al的金属性的强弱,a正确;
b.比较这两种元素的最高正化合价,只能说明它们原子的最外层电子数的多少,但与金属性强弱无关,b错误;
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液,说明Mg与水反应比Al与水反应更剧烈,故可以说明Mg和Al的金属性的强弱,c正确;
d.硬度和熔点属于物质的物理性质,金属性是化学性质,二者毫无联系,比较这两种金属的硬度和熔点不能比较出其金属性的强弱,d错误;
故答案为:ac;
II 从表列出了①~⑩10种元素在周期表中的位置可推知各元素分别为:①为Na,②为K,③为Mg,④为Al,⑤为C,⑥为N,⑦为P,⑧为Cl,⑨为Br,⑩为Ne;
(1)根据同一周期从左往右金属性减弱,同一主族从上往下金属性增强可知上述元素中,金属性最强的是K,同一周期从左往右原子半径逐渐减小,同一主族从上往下原子半径依次增大,故③④⑤三种元素的原子半径由大到小的顺序是Mg>Al>C,故答案为:K; Mg>Al>C;
(2)元素的非金属性越强,其最高价氧化物对应的水化物中酸性越强,同一周期从左往右非金属性增强,同一主族从上往下非金属性减弱,故上述元素的最高价氧化物对应的水化物中酸性最强的是HClO4,故答案为:HClO4;
(3)元素⑥是氮元素,其氢化物NH3的电子式为![]() ,该氢化物NH3与元素⑥的最高价氧化物对应的水化物HNO3反应的化学方程式为:NH3+HNO3=NH4NO3,故答案为:NH3+HNO3=NH4NO3。
,该氢化物NH3与元素⑥的最高价氧化物对应的水化物HNO3反应的化学方程式为:NH3+HNO3=NH4NO3,故答案为:NH3+HNO3=NH4NO3。

【题目】下列离子方程式能用来解释相应实验现象的是( )
实验现象 | 离子方程式 | |
A | 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 |
|
B | 向沸水中滴加饱和氯化铁溶液得到红褐色液体 |
|
C | 二氧化硫使酸性高锰酸钾溶液褪色 |
|
D | 氧化亚铁溶于稀硝酸 |
|
A. AB. BC. CD. D