题目内容
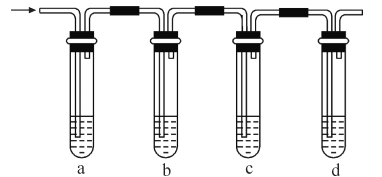
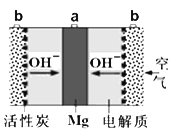
【题目】工业上可利用电解原理间接氧化法降解处理含有机污染物的废水,其原理如图所示,下列说法错误的是

A.介质离子在电极A上发生氧化反应,电极A为阳极
B.介质离子被氧化得到的强氧化剂可能为Cl2、O2
C.有机污染物在石墨电极上被还原为无污染物质
D.若介质离子为OH-,电极B上发生的反应为2H2O+2e-=H2↑+ 2OH-
【答案】C
【解析】
有A电极周围溶液中的介质离子被氧化为强氧化剂,可知电极A发生氧化反应,故电极A为电解池的阳极,B电极为阴极,阳极发生的电极反应为:2Cl--2e-=Cl2↑或4OH--4e-=O2↑+2H2O,阴极的电极反应为:2H2O+2e-=H2↑+2OH-;根据图示,有机物通过溶液中的氧化作用,被氧化为无污染的物质,从而得到降解,据此分析解答。
A.由电极A上失去电子,介质离子被氧化为强氧化剂,可知电极A为阳极,发生氧化反应,故A正确;
B.根据分析,溶液中的介质离子(Cl-、OH- )被氧化为Cl2、O2,故B正确;
C.根据分析,有机污染物通过与强氧化剂发生溶液中的氧化还原反应,被氧化为无污染的物质,并非在石墨电极.上被还原为无污染的物质,故C错误;
D.根据分析,电极B为阴极,发生还原反应,若介质离子为OH-,则电极B上发生的反应为2H2O+2e-=H2↑+2OH-,故D正确;
答案选C。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
反应I(热裂解):CH3COOH(g)2CO(g)+2H2(g) △H1
反应II(脱羧基):CH3COOH(g)CH4(g)+CO2(g) △H2
已知:反应I的活化能为(E5-E2)kJ,反应I逆反应的活化能为(E5-E3)kJ,反应II的活化能为(E4-E2)kJ,反应II逆反应的活化能为(E4-E1)kJ,E1到E5能量依次增大
(1)△H1+△H2=___________kJ/mol (用有关E的代数式表示);
(2)在不同温度下,向密闭容器中充入等量醋酸蒸汽,反应相同时间后,测得各气体的产率与温度的关系如图所示:

①约650℃之前,氢气产率低于甲烷的原因是;________________________________;
②约650℃之后,随着温度升高后,氢气产率高于甲烷的原因是:___________;(填编号)
a. 反应II速率减慢
b. 反应I速率加快的程度比反应II大
c. 反应I正向移动,而反应II逆向移动
d. 反应I正向移动的程度大于反应II正向移动的程度
③根据图像分析,该容器中一定发生了另外的副反应,理由是:______________。
(3)投入一定量的乙酸,在相同压强下,经过相同反应时间测得如下实验数据:
温度(℃) | 催化剂 | CH3COOH转化率 | H2的选择性 |
550 | 甲 | 14.5 | 40.2 |
550 | 乙 | 11.1 | 62.1 |
600 | 甲 | 11.2 | 41.2 |
600 | 乙 | 10.3 | 63.3 |
(H2的选择性:转化的CH3COOH中生成H2的百分比)
①表中实验数据表明,在相同温度下不同的催化剂对CH3COOH转化成H2的选择性有显著的影响,其原因是________。
②有利于提高CH3COOH转化为H2平衡转化率的措施有________。
A.使用催化剂甲 B.使用催化剂乙
C.升高反应温度 D.增加反应物的浓度
【题目】I.《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)l0Be和9Be_____________(填序号)。
a.是同一种原子 b.具有相同的中子数 c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:_________________________。
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是____________(填序号)。
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
II.下表列出了①~⑩10种元素在周期表中的位置。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑤ | ⑥ | ⑩ | |||||
3 | ① | ③ | ④ | ⑦ | ⑧ | |||
4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)________,③④⑤三种元素的原子半径由大到小的顺序是____________。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________(填化学式)
(3)元素⑥的氢化物的电子式为____________,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为_______________________________________。