题目内容
4.下列物质的电子式书写正确的是( )| A. |  | B. | 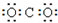 | C. |  | D. | 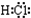 |
分析 A、水中O最外层满足8个电子的稳定结构;
B、CO2中C分别与O形成2对共价键;
C、氯化钠为离子化合物,氯离子核外电子没有标出;
D、HCl中Cl原子周围8个电子,H原子周围2个电子.
解答 解:A、H2O是共价化合物,是由原子和氢原子形成共价键,电子式为 ,故A错误;
,故A错误;
B、CO2中C分别与O形成2对共价键,电子式为: ,故B错误;
,故B错误;
C、氯化钠为离子化合物,氯离子带电荷并需用方括号括起来,钠离子用离子符号表示,电子式: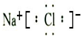 ,故C错误;
,故C错误;
D、HCl中Cl原子周围8个电子,H原子周围2个电子,所以HCl的电子式为: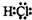 ,故D正确,故选D.
,故D正确,故选D.
点评 本题考查电子式的书写,难度不大,注意电子式中的电子数是指最外层电子数,而不是指电子总数,阴离子要写出离子的电子分布并加上括号和电荷.

练习册系列答案
相关题目
14.下列各原子或离子的电子排列式错误的是( )
| A. | Na+ 1s22s22p6 | B. | F- 1s22s22p6 | C. | N 1s22s22p3 | D. | O2-1s22s22p4 |
15.在不同条件下分别测得反应2SO2+O2?2SO3的化学反应速率,其中表示该反应进行得最快的是( )
| A. | v(SO2)=4 mol/(L•min) | B. | v(O2)=3 mol/(L•min) | ||
| C. | v(SO3)=6 mol/(L•min) | D. | v(O2)=6 mol/(L•min) |
19.已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol.下列关于中和热的说法中正确的是( )
| A. | 在稀溶液中所有酸和碱反应的中和热数值都相等 | |
| B. | 在稀溶液中1 mol酸和1 mol碱反应放出的热量都相等 | |
| C. | 在稀溶液中HCl和NaOH反应、HNO3和KOH反应的中和热相等 | |
| D. | 将浓硫酸滴入稍过量的氢氧化钠溶液中刚好生成1 mol水时,产生的热量即为中和热 |
9.25℃时,甲溶液的pH值为12,乙溶液的pH值为10,甲溶液与乙溶液中的C(OH-)之比是( )
| A. | 100 | B. | 1:100 | C. | 1:2 | D. | 2 |
16.下列反应的离子方程式中,书写正确的是( )
| A. | 实验室用大理石跟稀盐酸制取二氧化碳 2H++CO32-═CO2↑+H2O | |
| B. | 铁跟稀盐酸反应 2Fe+6H+═3H2↑+2Fe3+ | |
| C. | 氧化铝跟氢氧化钠溶液反应 Al2O3+OH-═AlO2-+H2O | |
| D. | 金属钠跟水反应 2Na+2H2O═2Na++2OH-+H2↑ |
13.下列说法正确的是( )
| A. | 化学反应不一定有分子碰撞 | |
| B. | 发生有效碰撞的分子是活化分子 | |
| C. | 化学反应一定需要活化能 | |
| D. | 只要普通分子具有合适的取向就能产生有效碰撞 |
15.下列物质分离实验方案的设计中,不可行的是( )
| A. | 用蒸馏的方法可以将海水淡化为可饮用水 | |
| B. | 用酒精萃取碘的水溶液中的碘 | |
| C. | 用分液的方法分离除去自来水中的固体悬浮杂质 | |
| D. | 加稀盐酸后过滤,除去混在铜粉中的少量锌粉 |