题目内容
【题目】下列说法不正确的是( )
A.铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,铅蓄电池在放电过程中,负极质量增加,正极质量也增加
B.金属铝的冶炼流程为: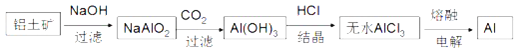
C.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D.一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
【答案】B
【解析】
A、铅蓄电池在放电过程中,Pb作负极,在反应中失去电子生成![]() ,反应式为:
,反应式为:![]() ,硫酸铅是固体,负极质量增重,正极电极反应式为
,硫酸铅是固体,负极质量增重,正极电极反应式为![]() ,正极质量增加,故A正确;
,正极质量增加,故A正确;
B、铝土矿的主要成分是![]() ,此外还含有少量
,此外还含有少量![]() 、
、![]() 等杂质,加入足量的氢氧化钠,氧化铝、二氧化硅与NaOH溶液反应均生成盐和水,只有氧化铁与碱不反应,过滤;滤液用二氧化碳酸化时,将硅酸钠和
等杂质,加入足量的氢氧化钠,氧化铝、二氧化硅与NaOH溶液反应均生成盐和水,只有氧化铁与碱不反应,过滤;滤液用二氧化碳酸化时,将硅酸钠和![]() 转化为硅酸和
转化为硅酸和![]() 沉淀,得不到纯净的氢氧化铝;另外不能通过电解熔融的氯化铝冶炼铝,故B错误;
沉淀,得不到纯净的氢氧化铝;另外不能通过电解熔融的氯化铝冶炼铝,故B错误;
C、常温下,铁和浓硝酸反应生成一层致密的氧化物薄膜而阻止了进一步反应,所以可以保护内部金属不被腐蚀,但加热反应剧烈,![]() (浓)
(浓)![]()
![]() ,故C正确;
,故C正确;
D、催化剂能降低反应所需的活化能,则能加快反应速率,但是不改变平衡,所以不改变平衡转化率,故D正确;
故选B。

 阅读快车系列答案
阅读快车系列答案【题目】下列有关硫、氮单质及其化合物的叙述正确的是( )
A.SO2、NO2均为酸性氧化物
B.“雷雨肥庄稼”与氮的固定有关
C.硫粉在过量的纯氧中燃烧可以生成SO3
D.亚硫酸钠可长期暴露在空气中,不易变质
【题目】下表是某同学探究Na2SO3溶液和铬(VI)盐溶液反应规律的实验记录,已知:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+
2CrO42-(黄色)+ 2H+
序号 | a | b | 现象 | |
| 1 | 2 mL 0.05 mol·L1 K2Cr2O7溶液(pH = 2) | 3滴饱和Na2SO3溶液(pH = 9) | 溶液变绿色(含Cr3+) |
2 | 2 mL 0.1 mol·L1 K2CrO4溶液(pH = 8) | 3滴饱和Na2SO3溶液 | 溶液没有明显变化 | |
3 | 2 mL饱和Na2SO3溶液 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变黄色 | |
4 | 2 mL蒸馏水 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变成浅橙色 |
下列说法不正确的是
A. 实验1中的绿色溶液中含有SO42-
B. 实验1、2的a溶液中所含的离子种类相同
C. 向实验3溶液中继续滴加过量硫酸可使溶液变为浅橙色
D. 实验4的目的是排除稀释对溶液颜色变化造成的影响