��Ŀ����
����Ŀ����������20 mL 0.1 mol��L-1 Na2CO3��Һ����μ���0.1 mol��L-1 HCl��Һ40 mL����Һ�к�̼Ԫ�صĸ�����(CO2���ݳ�δ����)���ʵ�������(����)����ҺpH�仯�IJ��������ͼ��ʾ��
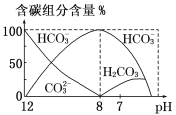
����˵����ȷ����
A. ��ͬһ��Һ�У�H2CO3��HCO3����CO32�����ܴ�������
B. ��pH��7ʱ����Һ�и�������(CO32������)�����ʵ���Ũ�ȵĴ�С��ϵΪ��c(Cl-)��c(Na+)��c(HCO3-)��c(H+)=c(OH-)
C. 0.1 mol/L Na2CO3��Һ��c(OH��)��c(H��)��c(H2CO3)��c(HCO3��)
D. �� pH��8ʱ��NaHCO3��Һ�����ʵ���Ũ��Ϊ0.1 mol/L
���𰸡�A
��������
A����ͼ��֪��pH��8��12ʱ����HCO3-��CO32-��pH��8����H2CO3��HCO3-����֪������Ӧ��ͬһ��Һ�У�H2CO3��HCO3-��CO32-���ܴ������棬��A��ȷ��
B����ͼ��֪��pH=7ʱc(H+)=c(OH-)����Һ����Ҫ����H2CO3��HCO3-����c(HCO3-)��c(H2CO3)��������ΪNaCl��NaHCO3��H2CO3�������c(Na+)��c(Cl-)��c(HCO3-)����B����
C��0.1 mol/L Na2CO3��Һ�д��ڵ���غ㣬c(Na+)+ c(H+)=2 c(CO32-)+ c(HCO3-)+ c(OH-)��Ҳ���������غ㣬c(Na+)=2[c(CO32-)+ c(HCO3-)+ c(H2CO3)]����c(OH��)��c(H��)��2c(H2CO3)+c(HCO3��)����C����
D���� pH��8ʱ��ǡ�÷�Ӧ����NaHCO3��Һ������������Һ�����Ϊ20mL����Һ�������40mL�����NaHCO3��Һ�����ʵ���Ũ����0.05 mol/L����D����
��ѡA��

����Ŀ��(1)��ͼ����ʵ�飬��a��Һ����ʢb��Һ���Թ��У�д���Թ��й۲쵽������Ӧ�����ӷ���ʽ��
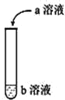
a | b | �Թ������� | ���ӷ���ʽ |
Na2CO3 | ϡ���� | ________________ | _________ |
ϡ���� | Na2CO3 | ______________ | _______________ |
(2)��ҵ������NaIO3��NaHSO3��Ӧ����ȡ����I2����ƽ���л�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶķ������Ŀ��
_____NaIO3+_____NaHSO3��_____I2+_____Na2SO4+_____H2SO4+_____H2O
(3)ClO2������ˮ�ľ�������ҵ�Ͽ���Cl2����NaClO2��Һ��ȡ![]() ��д���÷�Ӧ�����ӷ���ʽ������˫���ŷ���ʾ����ת�Ƶķ������Ŀ_____________________��
��д���÷�Ӧ�����ӷ���ʽ������˫���ŷ���ʾ����ת�Ƶķ������Ŀ_____________________��