题目内容
【题目】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是
A.生成40.0L N2(标准状况)B.有0.250mol KNO3被氧化
C.转移电子的物质的量为1.25molD.被氧化的N原子的物质的量为4.75mol
【答案】C
【解析】
该反应中N元素化合价由-![]() 、+5价变为0价,所以NaN3是还原剂、KNO3是氧化剂,N2既是氧化产物又是还原剂,根据反应方程式可知,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2molKNO3被还原,据此分析解答。
、+5价变为0价,所以NaN3是还原剂、KNO3是氧化剂,N2既是氧化产物又是还原剂,根据反应方程式可知,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2molKNO3被还原,据此分析解答。
A.该反应中N元素化合价由-![]() 价、+5价变为0价,所以氧化产物和还原产物都是氮气,假设有16mol氮气生成,氧化产物是15mol、还原产物是1mol,则氧化产物比还原产物多14mol,若氧化产物比还原产物多1.75mol,则生成氮气的物质的量=
价、+5价变为0价,所以氧化产物和还原产物都是氮气,假设有16mol氮气生成,氧化产物是15mol、还原产物是1mol,则氧化产物比还原产物多14mol,若氧化产物比还原产物多1.75mol,则生成氮气的物质的量=![]() ×16mol=2mol,标准状况下的体积为:2mol×22.4L/mol =44.8L,故A错误;
×16mol=2mol,标准状况下的体积为:2mol×22.4L/mol =44.8L,故A错误;
B.反应中,硝酸钾得电子是氧化剂,被还原,故B错误;
C.转移电子的物质的量为![]() ×10=1.25mol,故C正确;
×10=1.25mol,故C正确;
D.被氧化的N原子的物质的量=![]() ×30=3.75 mol,故D错误;
×30=3.75 mol,故D错误;
答案选C。

【题目】活性氧化锌是一种多功能性的新型无机材料。某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如图: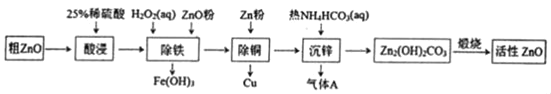
已知相关氢氧化物沉淀pH范围如表所示
Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀 | 5.4 | 7.0 | 2.3 | 4.7 |
完全沉淀 | 8.0 | 9.0 | 4.1 | 6.7 |
下列说法不正确的是( )
A.“酸浸”中25%稀硫酸可用98%浓硫酸配制,需玻璃棒、烧杯、量简、胶头滴管等仪器
B.“除铁”中用ZnO粉调节溶液pH至4.1~4.7
C.“除铜”中加入Zn粉过量对制备活性氧化锌的产量没有影响
D.“沉锌”反应为2Zn2++4HCO3﹣═Zn2(OH)2CO3↓+3CO2↑+H2O