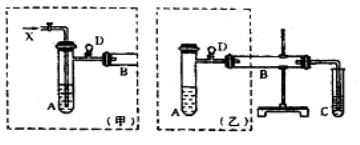题目内容
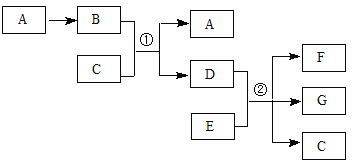
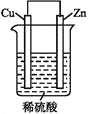
【题目】(14分)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请用如图实验装置,选用适当的化学试剂和实验用品,设计并完成对过氧化钠这一性质的探究。
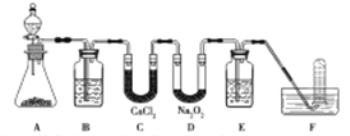
(1)A是实验室制取CO2的装置,其中发生反应的离子方程式是________;装置B的作用是____________。
(2)检验F中气体成分,即能说明过氧化钠可作潜水艇供氧剂,则实验操作的方法及现象是_______________。
(3)查阅有关资料表明:2H2O+2Na2O2=4NaOH+O2↑。某研究小组用同位素标记法对过氧化钠进行标记(![]() ),以探究这一反应的历程:_________________
),以探究这一反应的历程:_________________
①甲同学从电子转移角度得出其离子方程式为:_______________。
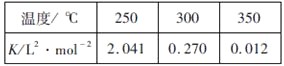
②乙同学发现:向Na2O2与水反应后的溶液中加入MnO2,又产生无色能使带火星的木条复燃的气体,从这个角度,写出其反应历程:___________________。
(4)设计并完成过氧化钠样品(已知所含杂质与酸碱均不反应)的纯度测定:
甲、乙两位同学各取了ag样品并分别配制成了100.00mL溶液进行实验,实验操作中甲同学是将样品直接溶于蒸馏水中;而乙同学却是将蒸馏水先加热煮沸,再把蒸馏水分成两份,一份中趁热加入样品溶解,待冷却到室温后再加人另一份水来进行配制。他们分别取出各自配制的溶液20.00mL,加入酚酞数滴后,用浓度为cmol/L的盐酸进行滴定;重复滴定操作2次,甲同学和乙同学分别计算出了所用盐酸的体积平均值,分别为VAmL和VWmL。
①在样品的溶解与配制中,你认为_______(填“甲”、“乙”)同学的操作是合理的,理由是:__________________。
②另一同学的操作将会使实验结果______(填“偏大”、“偏小”或“无影响”)。
③原过氧化钠样品的纯度是___________。
【答案】(1)CaCO3+2H+=Ca2++H2O+CO2↑(2分);除去CO2中混有的HCl(l分)
(2)待试管集满气体后,用大拇指堵住试管口从水槽中取出正立,松开拇指后,将带火星的木条迅速放在试管口,若木条复燃,则说明过氧化钠与二氧化碳反应产生氧气,可作供氧剂(2 分)
(3)①Na218O2+2H2O=4Na++2OH-+18O2↑+218OH-
②2H2O+Na218O2=2NaOH+ H218O2;2H218O2![]() 2H218O+ 18O2↑
2H218O+ 18O2↑
(4)①乙;沸水能使Na2O2溶解时所生成的H2O2迅速分解,消除其对中和滴定(特别是指示剂)的影响;②偏小 ③![]()
【解析】
试题分析:(1)A是实验室制取CO2的装置,其中发生反应的离子方程式是CaCO3+2H+=Ca2++H2O+CO2↑;由于盐酸易挥发,生成的二氧化碳中含有氯化氢气体,因此装置B的作用是除去CO2中混有的HCl。
(2)二氧化碳与过氧化钠反应生成氧气,氧气是助燃性气体,则检验F中气体成分的实验操作的方法及现象是待试管集满气体后,用大拇指堵住试管口从水槽中取出正立,松开拇指后,将带火星的木条迅速放在试管口,若木条复燃,则说明过氧化钠与二氧化碳反应产生氧气,可作供氧剂。
(3)①过氧化钠与水的反应中过氧化钠既是氧化剂,也是还原剂,则从电子转移角度得出其离子方程式为Na218O2+2H2O=4Na++2OH-+18O2↑+218OH-。
②向Na2O2与水反应后的溶液中加入MnO2,又产生无色能使带火星的木条复燃的气体,这说明反应中有双氧水生成,双氧水在二氧化锰的作用下分解生成氧气,其反应历程可表示为2H2O+Na218O2=2NaOH+ H218O2;2H218O2![]() 2H218O+ 18O2↑。
2H218O+ 18O2↑。
(4)①由于沸水能使Na2O2溶解时所生成的H2O2迅速分解,消除了双氧水对中和滴定(特别是指示剂)的影响,所以乙的操作方法正确;
②由于酚酞能够消耗氢氧化钠溶液,则滴定过程中消耗盐酸的体积偏小,测定结果偏小;
③乙的操作合理,若100mL配制的样品溶液完全用该浓度的盐酸中和,消耗盐酸体积应该为:(VWmL×100mL)/ 20mL=5VWmL,消耗氯化氢的物质的量为:cmol/L×5VW×10-3L=5cVW×10-3mol,则样品中含有氢氧化钠的物质的量为:5cVW×10-3mol,过氧化钠的物质的量为:0.5×5cVW×10-3mol=2.5cVW×10-3mol,样品的纯度为:(78g/mol×2.5cVW×10-3mol)/ag×100%=![]() 。
。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案