题目内容
【题目】缺电子化合物是指电子数不符合路易斯结构(一个原子通过共享电子使其价层电子数达到8,H原子达到2所形成的稳定分子结构)要求的一类化合物。下列说法错误的是
A.NH3、BF3、BF4-中只有BF3是缺电子化合物
B.BF3、BF4-中心原子的杂化方式分别为sp2、sp3
C.BF3与NH3反应时有配位键生成
D.BF4-的键角小于NH3
【答案】D
【解析】
A. NH3电子式为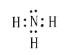 符合路易斯结构,BF3电子式为
符合路易斯结构,BF3电子式为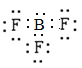 ,B原子价层电子数为6,不符合路易斯结构、BF4-电子式为
,B原子价层电子数为6,不符合路易斯结构、BF4-电子式为 ,只有BF3是缺电子化合物,故A正确;
,只有BF3是缺电子化合物,故A正确;
B. BF3中心原子B价层电子对数为![]() ,则杂化方式为sp2杂化;BF4-中心原子B价层电子对数为
,则杂化方式为sp2杂化;BF4-中心原子B价层电子对数为![]() ,则杂化方式分别为sp3杂化,故B正确;
,则杂化方式分别为sp3杂化,故B正确;
C. BF3与NH3反应时,NH3中N原子有孤电子对,BF3中B有空轨道,可生成配位键,故C正确;
D. BF4-和NH3均为sp3杂化, BF4-中心原子无孤电子对,NH3有一对孤电子对,根据价层电子对互斥理论,孤电子对数增多,对成键电子的斥力增大,键角减小,则BF4-的键角大于NH3,故D错误;
故答案选:D。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】回答下列问题
(1)等pH、等体积的两份溶液A(盐酸)和B(CH3COOH)分別与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_____(填写序号)。
①开始反应时的速率A>B ②参加反应的锌的物质的量A=B
③反应所需要的时间B>A ④A中有锌剩余
(2)已知,CH3COOH是常见的弱酸,现有常温下0.1molL-1的CH3COOH溶液。
①温度不变,加水稀释过程中,下列表达式的数据一定变小的是_____(填字母序号,下同),②若该溶液升高温度,下列表达式的数据增大的是_____。
A.c(H+) B.c(H+)·c(OH-)
C.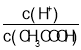 D.
D.![]()
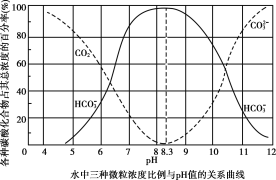
(3)取0.10mol CH3COOH(冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):
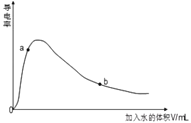
① n(H+):a_____b;
② c(CH3COO-):a_____b;
③完全中和时消耗NaOH的物质的量:a_____b;
(4)25℃时,部分物质的电离平衡常数如下表所示:
CH3COOH | H2CO3 | HCN |
1.7×10﹣5 | K1=4.3×10-7 K2=5.6×10﹣11 | 4.9×10﹣10 |
请回答下列问题:
① CH3COOH、H2CO3、HCN的酸性由强到弱的顺序为_________。
② 焦炉煤气中一般含有H2S和HCN气体,有的工厂在真空条件下,使用K2CO3溶液吸收煤气中的H2S和HCN气体,实现脱硫脱氰。请根据上述数据,尝试从理论上推测同为0.l molL-1的K2CO3溶液和HCN混合后,最可能发生的反应的离子方程式_____。
【题目】使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到___________(填仪器名称)中定容,摇匀即得。
(2)用________取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴___作指示剂。
(3)读取盛装0.1000 mol/L NaOH 溶液的___________(填仪器名称)的初始读数。如果液面位置如图所示,则此时的读数为_________mL。
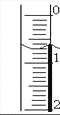
(4)滴定。当______________________________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(1)经计算,市售白醋总酸量=_____________g/100mL。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是______(填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出