题目内容
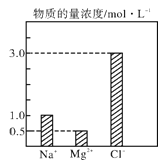
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,1个氧气分子体积为 ![]() cm3
cm3
B.铜电解精炼时,当阳极质量减少64 g时,电路中转移电子数为2NA
C.标准状况下22.4 L Cl2完全溶于水时,所得溶液中含氯微粒总数为2NA
D.NaCl晶体中Na+与最近Cl-的核间距离为a cm,则其晶体密度为 ![]() g·cm-3
g·cm-3
【答案】D
【解析】
A. 标准状况下,1个氧气分子体积由氧气分子的大小决定不能直接用气体摩尔体积进行计算,故A错误;
B. 铜电解精炼时,阳极中含有Cu、Fe、Zn等金属,Fe、Zn先放电,当阳极质量减少64 g时,电路中转移电子数不等于2NA,故B错误;
C. 标准状况下22.4 L Cl2物质的量为1mol完全溶于水时,所得溶液中含氯微粒有Cl2、HClO、Cl-、ClO-,根据氯原子守恒可知:![]() , 则含氯微粒总数小于2NA,故C错误;
, 则含氯微粒总数小于2NA,故C错误;
D. NaCl晶胞中Na+数目为![]() , Cl-数目为
, Cl-数目为![]() ,则晶胞质量为:
,则晶胞质量为:![]() ,与最近Cl-的核间距离为a cm,则体积为
,与最近Cl-的核间距离为a cm,则体积为![]() ,则其晶体密度为
,则其晶体密度为 ![]() g·cm-3,故D正确;
g·cm-3,故D正确;
故答案选:D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目