题目内容
【题目】在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是
A.v(NH3)=0.05 mol/(Lmin)B.v(NH3)=0.2 mol/(Lmin)
C.v(H2)=0.3 mol/(Lmin)D.v(H2)=0.4 mol/(Lmin)
【答案】D
【解析】
同一化学反应中,同一时间段内,各物质的反应速率之比等于其计量数之比;先把不同物质的反应速率换算成同一物质的反应速率进行比较,从而确定选项。
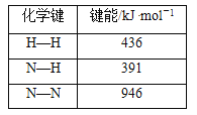
反应为N2(g)+3H2(g)![]() 2NH3(g),以N2的反应速率为标准进行判断。
2NH3(g),以N2的反应速率为标准进行判断。
A.v(NH3)=0.05 mol/(Lmin),所以v(N2)=0.025 mol/(Lmin);
B.v(NH3)=0.2 mol/(Lmin),所以v(N2)=0.1 mol/(Lmin);
C.v(H2)=0.3 mol/(Lmin),所以v(N2)=0.1 mol/(Lmin);
D.v(H2)=0.4 mol/(Lmin),所以v(N2)=![]() mol/(Lmin)>0.1 mol/(Lmin),所以反应速率最快的是
mol/(Lmin)>0.1 mol/(Lmin),所以反应速率最快的是![]() mol/(Lmin),故合理选项是D。
mol/(Lmin),故合理选项是D。

 名校课堂系列答案
名校课堂系列答案【题目】电解质的水溶液中存在电离平衡。
Ⅰ.(1)醋酸是常见的弱酸。下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是_____(填字母序号)。
a 滴加少量浓盐酸 b 微热溶液 c 加水稀释 d 加入少量醋酸钠晶体
Ⅱ.白醋是常见的烹调酸味辅料,白醋总酸度测定方法如下。
a 量取20.00 mL白醋样品,用100 mL容量瓶配制成待测液。
b 将滴定管洗净、润洗,装入溶液,赶出尖嘴处气泡,调整液面至0刻度线。
c 取20.00 mL配制的待测液于洁净的锥形瓶中,加3滴酚酞溶液,用0.1000 mol· L-1的NaOH溶液滴定至终点,记录数据。
d 重复滴定实验3次并记录数据。
e 计算白醋样品中醋酸总酸度。回答下列问题:
(2)实验a中量取20.00 mL白醋所用的仪器名称是___________。
(3)若实验b中碱式滴定管未用NaOH标准溶液润洗,会造成测定结果比准确值_________(填“偏大”、“偏小”或“不变”)。
(4)实验C中判断滴定终点的现象是_______。
(5)实验数据如下表,则该白醋样品中醋酸总酸度为_________ mol· L-1。
待测液体积/mL | 标准NaOH溶液 | ||
滴定前读数/mL | 滴定终点读数/mL | ||
第1次 | 20.00 | 0 | 21.98 |
第2次 | 20.00 | 0 | 22.00 |
第3次 | 20.00 | 0 | 22.02 |
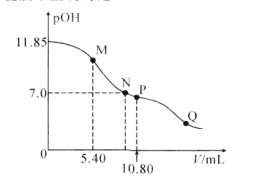
Ⅲ.25℃,向20.00 mL 0.100 0 mol·L1 CH3COOH中滴加0.100 0 mol·L-1 NaOH过程中,pH变化如下图所示。
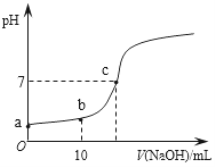
(6)a点溶液pH > 1,用电离方程式解释原因:_____________。
(7)下列有关b点溶液的说法正确的是_______(填字母序号)。
a 溶质为:CH3COOH、CH3COONa
b 微粒浓度满足:c(Na+) + c(H+) = c(CH3COO-) + c(OH)
c 微粒浓度满足:c(Na+) = c(CH3COOH) + c(CH3COO-)
d 微粒浓度满足:2c(H+) + c(CH3COO-) =2c(OH-) +c(CH3COOH)
(8)c点溶液中离子浓度的大小顺序:__________。