题目内容
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Na与乙醇完全反应,失去2NA电子 |
| B、常温常压下,16g CH4含有10NA个电子 |
| C、1L 0.1mol?L-1的醋酸溶液中含有0.1NA个H+ |
| D、标准状况下,22.4L苯含有NA个苯分子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.钠为1价金属,1mol钠完全反应失去1mol电子;
B.甲烷中含有10个电子,16g甲烷的物质的量为1mol,含有10mol电子;
C.醋酸为弱电解质,溶液中醋酸只能部分电离出氢离子;
D.标准状况下,苯的状态不是气体,不能使用标况下的气体摩尔体积计算苯的物质的量.
B.甲烷中含有10个电子,16g甲烷的物质的量为1mol,含有10mol电子;
C.醋酸为弱电解质,溶液中醋酸只能部分电离出氢离子;
D.标准状况下,苯的状态不是气体,不能使用标况下的气体摩尔体积计算苯的物质的量.
解答:
解:A.1mol钠与乙醇完全反应失去1mol电子,失去NA电子,故A错误;
B.16g甲烷的物质的量为1mol,1mol甲烷中含有10mol电子,含有10NA个电子,故B正确;
C.1L 0.1mol?L-1的醋酸溶液中含有醋酸0.1mol,0.1mol醋酸电离出的氢离子小于0.1mol,溶液中含有的氢离子小于0.1NA,故C错误;
D.标况下苯不是气体,不能使用标况下的气体摩尔体积计算22.4L苯的物质的量,故D错误;
故选B.
B.16g甲烷的物质的量为1mol,1mol甲烷中含有10mol电子,含有10NA个电子,故B正确;
C.1L 0.1mol?L-1的醋酸溶液中含有醋酸0.1mol,0.1mol醋酸电离出的氢离子小于0.1mol,溶液中含有的氢离子小于0.1NA,故C错误;
D.标况下苯不是气体,不能使用标况下的气体摩尔体积计算22.4L苯的物质的量,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标准状况下苯不是气体,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
 科研、生产中常涉及钠、硫及其化合物.如图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,下列叙述错误的是( )
科研、生产中常涉及钠、硫及其化合物.如图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,下列叙述错误的是( )| A、该电池的负极材料是钠 |
| B、陶瓷材料的作用是导电(电解质)兼隔膜 |
| C、当电池中转移1.204×1024个电子时,消耗钠的物质的量为2mol |
| D、外电路中电子的移动方向是:S→Na |
X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见气体甲.X、Y、Z 3种元素形成化合物乙.下列说法不正确的是( )
| A、原子半径:W>Y>Z>M>X |
| B、化合物乙中一定只有共价键 |
| C、由W元素形成的单质以及W与Z两元素形成的化合物都是原子晶体 |
| D、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |
下列物质的水溶液中,除水分子外,不存在其他分子的是( )
| A、H3PO4 |
| B、NaF |
| C、HNO3 |
| D、KHS |
在某未知溶液中检验出含有Ba2+、NO3-,且溶液的pH=1.某学生还需鉴定此溶液中是否大量存在①Al3+ ②NH4+ ③Fe2+ ④Cl- ⑤AlO2- ⑥SO42- 其实这些离子中有一部分不必再鉴定就能加以否定,你认为不必再鉴定的离子组是( )
| A、③⑤⑥ | B、④⑤⑥ |
| C、①②⑤ | D、①③④ |
X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法错误的是( )
| A、气态氢化物稳定性:HmW>HnR |
| B、标准状况下,1mol XW4的体积约为22.4L |
| C、Y和Z形成的某种化合物中含离子键、非极性健 |
| D、Y、Z、R三者形成的某种化合物溶于水后,可形成碱性溶液 |
原电池反应是释放能量的氧化还原反应,下列可设计成原电池的化学反应是( )
| A、H2O (l)+CaO(s)═Ca(OH)2(s) | ||||
| B、Ba(OH)2?8H2O+2NH4Cl═BaCl2+2NH3?H2O+8H2O | ||||
C、2KClO3
| ||||
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(l) |
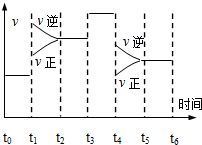 2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.
2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.