��Ŀ����
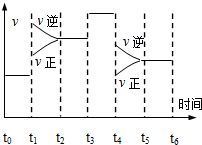 2013�궬�����������������Ű�ҹ�������������������β������ɿ�����Ⱦ��ԭ��֮һ���о���������β����Ϊ������������Ҫ����
2013�궬�����������������Ű�ҹ�������������������β������ɿ�����Ⱦ��ԭ��֮һ���о���������β����Ϊ������������Ҫ������1��������ȼ������ʱ������Ӧ��N2��g��+O2��g��?2NO��g�����ǵ�������β���к���NO��ԭ��֮һ����ij���������и÷�Ӧ��ʼ���ﵽƽ��Ĺ����У����и�����仯����
A�����������ܶ� B����������ѹǿ
C������Ӧ���� D����λʱ���ڣ�����N2������NO�����ʵ���֮��
��2����������β���ķ���֮һ�����������ϰ�װ��ת�������������·�Ӧ��
2NO��g��+2CO��g��
| ���� |
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=
����һ���¶��£���2mol NO��1mol CO����1L�̶��ݻ��������У���5min��ﵽƽ��״̬��CO2��ƽ����Ӧ����v ��CO2��=0.1mol?��L?min��-1����NO��ת������
����ͼ�Ƿ�Ӧ2NO��g��+2CO��g��
| ���� |
��3�������������շ�Ҳ���Գ�ȥNO��������NO�в��������������γ���NO��NO2��ɵ�������û������n��NO����n��NO2��=1��3�����������ͨ��ʯ�����У�ʹ֮ת��Ϊ����ƣ�
��д���������շ���ȥ��������Ļ�ѧ����ʽ
�����б�״���µ�O2 33.6mL�������Ͽ��Դ����õ�������
���㣺��ѧ��Ӧ�����뻯ѧƽ��ͼ����ۺ�Ӧ��,��ѧƽ�ⳣ���ĺ���,��ѧƽ���Ӱ������
ר�⣺��ѧƽ��ר��
��������1��A�������������������䣬������������䣬���������ܶ�ʼ�ղ��䣻
B����������ܵ����ʵ������䣬����������䣬�ݴ��жϣ�
C���淴Ӧ���У���Ӧ��Ũ�Ƚ��ͣ�����Ӧ�������ͣ�
D���淴Ӧ���У���Ӧ��Ũ�Ƚ��ͣ�����Ӧ�������ͣ��������Ũ�������淴Ӧ�������ʵ�λʱ���ڣ�N2����������С��NO������������
��2���ٸ��ݷ�Ӧ����ʽ2NO��g��+2CO��g��
2CO2��g��+N2��g����ƽ�ⳣ���ĸ���д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��
���ȸ��ݴﵽƽ��ʱ����ֵ�Ũ�ȼ�������¶��µ�ƽ�ⳣ����Ȼ����ݳ���CO 0.5mol��N2 0.75mol�����ֵ�Ũ�ȼ����Ũ���̣�����������ƽ�ⳣ����Ƚϣ��Ӷ��жϻ�ѧƽ���Ƿ��ƶ����ƶ�����
��t4ʱ�����淴Ӧ����ͬʱ��С�������Ǽ�Сѹǿ���߽����¶ȣ�����v���棩��v��������ƽ�����������ƶ���˵���Ǽ�С��ѹǿ��
��3����n��NO����n��NO2��=1��3����Ӧ���ɲ���Ϊ��������ӣ����ݻ��ϼ����������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��
�ڸ��ݷ�Ӧ����ʽ������������������Ӧ����һ�������Ͷ����������������
B����������ܵ����ʵ������䣬����������䣬�ݴ��жϣ�
C���淴Ӧ���У���Ӧ��Ũ�Ƚ��ͣ�����Ӧ�������ͣ�
D���淴Ӧ���У���Ӧ��Ũ�Ƚ��ͣ�����Ӧ�������ͣ��������Ũ�������淴Ӧ�������ʵ�λʱ���ڣ�N2����������С��NO������������
��2���ٸ��ݷ�Ӧ����ʽ2NO��g��+2CO��g��
| ���� |
���ȸ��ݴﵽƽ��ʱ����ֵ�Ũ�ȼ�������¶��µ�ƽ�ⳣ����Ȼ����ݳ���CO 0.5mol��N2 0.75mol�����ֵ�Ũ�ȼ����Ũ���̣�����������ƽ�ⳣ����Ƚϣ��Ӷ��жϻ�ѧƽ���Ƿ��ƶ����ƶ�����
��t4ʱ�����淴Ӧ����ͬʱ��С�������Ǽ�Сѹǿ���߽����¶ȣ�����v���棩��v��������ƽ�����������ƶ���˵���Ǽ�С��ѹǿ��
��3����n��NO����n��NO2��=1��3����Ӧ���ɲ���Ϊ��������ӣ����ݻ��ϼ����������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��
�ڸ��ݷ�Ӧ����ʽ������������������Ӧ����һ�������Ͷ����������������
���
�⣺��1��A�������������������䣬������������䣬���������ܶȲ��䣬��A����
B����������ܵ����ʵ������䣬����������䣬��������ѹǿ���䣬��B����
C�����ŷ�Ӧ�Ľ��У���Ӧ��Ũ�Ƚ��ͣ�������Ӧ�������ͣ���C��ȷ��
D���淴Ӧ���У���Ӧ��Ũ�Ƚ��ͣ�����Ӧ�������ͣ��������Ũ�������淴Ӧ�������ʵ�λʱ���ڣ�N2����������С��NO������������λʱ���ڣ�N2��NO��������֮�ȼ�С������ȷ��
�ʴ�Ϊ��CD��
��2���ٷ�Ӧ����ʽ2NO��g��+2CO��g��
2CO2��g��+N2��g���Ļ�ѧƽ�ⳣ������ʽΪ��K=
��
�ʴ�Ϊ��
��
����5min��ﵽƽ��״̬��CO2��ƽ����Ӧ����v ��CO2��=0.1mol?��L?min��-1����Ӧ���ɶ�����̼��Ũ��Ϊ��0.1mol?��L?min��-1��5min=0.5mol/L����Ӧ����NO��Ũ��Ϊ��c��NO��=c��CO2��=0.5mol/L��
����NO��ת����Ϊ��
��100%=25%��
�ﵽƽ��ʱ����ֵ�Ũ�ȷֱ�Ϊ��c��CO2��=0.5mol/L��c��NO��=
-0.5mol/L=1.5mol/L��c��N2��=0.25mol/L��c��CO��=
-0.5mol/L=0.5mol/L������¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ��K=
=
��
������ƽ��������г���CO 0.5mol��N2 0.75mol��COŨ�ȱ�Ϊ��c��CO��=0.5mol/L+
=1mol/L��������Ũ��Ϊ��c��N2��=0.25mol/L+
=1mol/L�����ʱ��Ũ����Ϊ��
=1
mol=
=K�����Ի�ѧƽ�ⲻ�����ƶ���
�ʴ�Ϊ��25%������
�۸���ͼ���֪��t4ʱ�����淴Ӧ���ʶ�ͬʱ��С�������Ǽ�Сѹǿ���߽����¶ȣ��������¶ȣ��÷�Ӧ�����ȷ�Ӧ��ƽ�����������ƶ�����t4ʱ��v���棩��v��������ƽ�����������ƶ���˵���Ǽ�С��ѹǿ��
�ʴ�Ϊ����Сѹǿ��
��3���������������շ�Ҳ���Գ�ȥNO��������NO�в��������������γ���NO��NO2��ɵ�������û������n��NO����n��NO2��=1��3�����������ͨ��ʯ�����У�ʹ֮ת��Ϊ����ƣ���һ������Ϊ1mol�����������Ϊ3mol��1molһ������ת�������������ʧȥ3mol���ӣ�3mol��������ת��������ʧȥ3mol���ӣ��ܹ�ʧȥ6mol���ӣ���Ҫ�������������ʵ���Ϊ
=1.5mol�����ڻ�ѧ����ʽ�в��ܳ��ַ����������������ļ�����Ϊ3��һ�������Ͷ��������ļ������ֱ�Ϊ2��6���÷�Ӧ�Ļ�ѧ����ʽΪ��3O2+2NO+6NO2+4Ca��OH��2=4Ca��NO3��2+4H2O��
�ʴ�Ϊ��3O2+2NO+6NO2+4Ca��OH��2=4Ca��NO3��2+4H2O��
�ڷ�Ӧ����ʽ��3O2+2NO+6NO2+4Ca��OH��2=4Ca��NO3��2+4H2O
3 2 6
33.6mL x y��
��ã�x=22.4mL��y=67.2mL��
���״���µ�O2 33.6mL�������Ͽ��Դ����õ����������Ϊ��22.4mL+67.2mL=89.6mL��
�ʴ�Ϊ��89.6mL��
B����������ܵ����ʵ������䣬����������䣬��������ѹǿ���䣬��B����
C�����ŷ�Ӧ�Ľ��У���Ӧ��Ũ�Ƚ��ͣ�������Ӧ�������ͣ���C��ȷ��
D���淴Ӧ���У���Ӧ��Ũ�Ƚ��ͣ�����Ӧ�������ͣ��������Ũ�������淴Ӧ�������ʵ�λʱ���ڣ�N2����������С��NO������������λʱ���ڣ�N2��NO��������֮�ȼ�С������ȷ��
�ʴ�Ϊ��CD��
��2���ٷ�Ӧ����ʽ2NO��g��+2CO��g��
| ���� |
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
�ʴ�Ϊ��
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
����5min��ﵽƽ��״̬��CO2��ƽ����Ӧ����v ��CO2��=0.1mol?��L?min��-1����Ӧ���ɶ�����̼��Ũ��Ϊ��0.1mol?��L?min��-1��5min=0.5mol/L����Ӧ����NO��Ũ��Ϊ��c��NO��=c��CO2��=0.5mol/L��
����NO��ת����Ϊ��
| 0.5mol/L | ||
|
�ﵽƽ��ʱ����ֵ�Ũ�ȷֱ�Ϊ��c��CO2��=0.5mol/L��c��NO��=
| 2mol |
| 1L |
| 1mol |
| 1L |
| 0.25��0��55 |
| 0��52��1��52 |
| 1 |
| 9 |
������ƽ��������г���CO 0.5mol��N2 0.75mol��COŨ�ȱ�Ϊ��c��CO��=0.5mol/L+
| 0.5mol |
| 1L |
| 0.75mol |
| 1L |
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
| 1��0��52 |
| 12��1��52 |
| 1 |
| 9 |
�ʴ�Ϊ��25%������
�۸���ͼ���֪��t4ʱ�����淴Ӧ���ʶ�ͬʱ��С�������Ǽ�Сѹǿ���߽����¶ȣ��������¶ȣ��÷�Ӧ�����ȷ�Ӧ��ƽ�����������ƶ�����t4ʱ��v���棩��v��������ƽ�����������ƶ���˵���Ǽ�С��ѹǿ��
�ʴ�Ϊ����Сѹǿ��
��3���������������շ�Ҳ���Գ�ȥNO��������NO�в��������������γ���NO��NO2��ɵ�������û������n��NO����n��NO2��=1��3�����������ͨ��ʯ�����У�ʹ֮ת��Ϊ����ƣ���һ������Ϊ1mol�����������Ϊ3mol��1molһ������ת�������������ʧȥ3mol���ӣ�3mol��������ת��������ʧȥ3mol���ӣ��ܹ�ʧȥ6mol���ӣ���Ҫ�������������ʵ���Ϊ
| 6mol |
| 4 |
�ʴ�Ϊ��3O2+2NO+6NO2+4Ca��OH��2=4Ca��NO3��2+4H2O��
�ڷ�Ӧ����ʽ��3O2+2NO+6NO2+4Ca��OH��2=4Ca��NO3��2+4H2O
3 2 6
33.6mL x y��
��ã�x=22.4mL��y=67.2mL��
���״���µ�O2 33.6mL�������Ͽ��Դ����õ����������Ϊ��22.4mL+67.2mL=89.6mL��
�ʴ�Ϊ��89.6mL��
���������⿼���˻�ѧ��Ӧ�����뻯ѧƽ��ͼ����ۺ����á���ѧƽ�ⳣ���ļ��㡢������ԭ��Ӧ����ʽ����д��֪ʶ����Ŀ�ѶȽϴ�����ļ������ϴ��漰��֪ʶ��϶࣬��ֿ�����ѧ���ķ������������������Ӧ����ѧ֪ʶ����������2����Ϊ�ѵ㣬ע���ȼ������ѧƽ�ⳣ����Ȼ���ٸ���Ũ�����ж�ƽ���ƶ�����

��ϰ��ϵ�д�
 ������ϵ�д�
������ϵ�д�
�����Ŀ
��NAΪ�����ӵ���������ֵ������˵����ȷ���ǣ�������
| A��1mol Na���Ҵ���ȫ��Ӧ��ʧȥ2NA���� |
| B�����³�ѹ�£�16g CH4����10NA������ |
| C��1L 0.1mol?L-1�Ĵ�����Һ�к���0.1NA��H+ |
| D����״���£�22.4L������NA�������� |
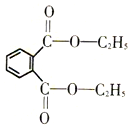 �ڱ�������������һ����ʹ�������������ܼ���������Ӱ��̥����Ӥ�����ںɶ��ɷ��ڣ���������ʧ�������¶�ͯ�����죬�ǿ����°�����й����ڱ���������������ṹ��ͼ��ʾ����˵������ȷ���ǣ�������
�ڱ�������������һ����ʹ�������������ܼ���������Ӱ��̥����Ӥ�����ںɶ��ɷ��ڣ���������ʧ�������¶�ͯ�����죬�ǿ����°�����й����ڱ���������������ṹ��ͼ��ʾ����˵������ȷ���ǣ�������| A��������ˮ���������Ҵ���������л��ܼ� |
| B�����ܷ����ӳɷ�Ӧ��Ҳ�ܷ���ȡ����Ӧ |
| C��1mol������ǡ������2mol NaOH��ȫ��Ӧ |
| D��0.1mol�����ʳ��ȼ����Ҫ��״��������32L |
ij�����Ľṹ��ʽΪ�� ������������ȷ���ǣ�������
������������ȷ���ǣ�������
 ������������ȷ���ǣ�������
������������ȷ���ǣ�������| A��2��3-�������� |
| B��2-3-�������� |
| C��2-��-3-�һ����� |
| D��2-�һ�-3-������ |
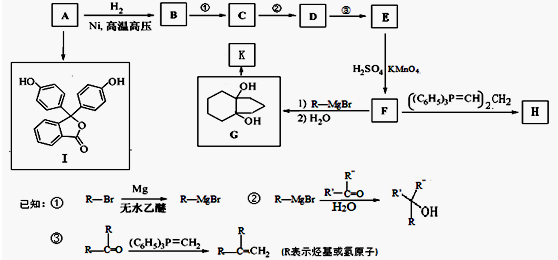
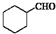 �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�