题目内容
X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法错误的是( )
| A、气态氢化物稳定性:HmW>HnR |
| B、标准状况下,1mol XW4的体积约为22.4L |
| C、Y和Z形成的某种化合物中含离子键、非极性健 |
| D、Y、Z、R三者形成的某种化合物溶于水后,可形成碱性溶液 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、R、W是5种短周期元素,原子序数依次增大.Y、R同主族,且形成共价化合物RY3,则R为S元素,Y为O元素;离子化合物Z2Y中Y的化合价为-2价,则Z的化合价为+1价,Z为ⅠA族元素,Z、R、W同周期,即处于第三周期,则Z为Na元素;W原子序数最大,则W是Cl元素,X原子序数小于O氧元素,结合XW4可知X为C元素,以此解答.
解答:
解:X、Y、Z、R、W是5种短周期元素,原子序数依次增大.Y、R同主族,且形成共价化合物RY3,则R为S元素,Y为O元素;离子化合物Z2Y中Y的化合价为-2价,则Z的化合价为+1价,Z为ⅠA族元素,Z、R、W同周期,即处于第三周期,则Z为Na元素;W原子序数最大,则W是Cl元素,X原子序数小于O氧元素,结合XW4可知X为C元素,
A.非金属性Cl>S,则氢化物稳定性HCl>H2S,故A正确;
B.标况下,CCl4是液态,不能用气体摩尔体积计算其体积,故B错误;
C.Y、Z元素组成的化合物有Na2O、Na2O2,而Na2O2中既含有离子键又含有共价键,故C正确;
D.Y、Z、R三种元素组成的化合物有Na2SO3、Na2SO4等,其溶液分别呈碱性和中性,故D正确,
故选B.
A.非金属性Cl>S,则氢化物稳定性HCl>H2S,故A正确;
B.标况下,CCl4是液态,不能用气体摩尔体积计算其体积,故B错误;
C.Y、Z元素组成的化合物有Na2O、Na2O2,而Na2O2中既含有离子键又含有共价键,故C正确;
D.Y、Z、R三种元素组成的化合物有Na2SO3、Na2SO4等,其溶液分别呈碱性和中性,故D正确,
故选B.
点评:本题考查位置结构性质的相互关系应用,题目难度中等,同主族元素Y、R形成的化学式是推断突破口,再根据物质的化学式判断元素的化合价确定元素.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
等物质的量的下列物质完全燃烧时,消耗氧气的量最多的是( )
| A、C2H4 |
| B、C2H6 |
| C、C2H5OH |
| D、CH3COOH |
下列有关元素周期表的说法中,正确的是( )
| A、能生成碱的金属元素都在ⅠA族 |
| B、原子序数为14的元素位于元素周期表的第3周ⅥA族 |
| C、稀有气体元素原子的最外层电子数为2或8 |
| D、元素周期表有18个纵行,分列16个族,即7个主族、8个副族和1个0族 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Na与乙醇完全反应,失去2NA电子 |
| B、常温常压下,16g CH4含有10NA个电子 |
| C、1L 0.1mol?L-1的醋酸溶液中含有0.1NA个H+ |
| D、标准状况下,22.4L苯含有NA个苯分子 |
将铝条插入盛有CuCl2浓溶液的烧杯,反应过程中一定不可能出现的现象是( )
| A、产生无色气体 |
| B、产生蓝色絮状沉淀 |
| C、紫红色固体析出 |
| D、黄绿色气泡逸出 |
化学与工农业生产和人类生活密切相关.下列说法中,不正确的是( )
| A、油脂在碱性条件下水解可制得肥皂 |
| B、海轮外壳上镶入锌块,可减缓船体的腐蚀 |
| C、人体中缺碘元素会得贫血病 |
| D、研制推广甲醇燃料汽车,有利于“减排目标”的实现 |
25℃时,弱酸的电离平衡常数如表所示,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等物质的量浓度溶液pH关系:pH(CH3COONa)<pH(NaHCO3)<pH(NaCN) |
| B、a mol?L-1 HCN与b mol?L-1 NaOH溶液等体积混合后溶液中c(Na+)>c(CN-),则a一定小于b |
| C、0.1mol?L-1的CH3COOH的 pH比0.1mol?L-1 HCN的pH大 |
| D、NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
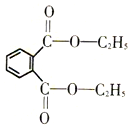 邻苯二甲酸酯类是一类能使塑料柔软的增塑剂,它可能影响胎儿和婴幼儿体内荷尔蒙分泌,引发激素失调,导致儿童性早熟,是可疑致癌物.下列关于邻苯二甲酸二乙酯(结构如图所示)的说法不正确的是( )
邻苯二甲酸酯类是一类能使塑料柔软的增塑剂,它可能影响胎儿和婴幼儿体内荷尔蒙分泌,引发激素失调,导致儿童性早熟,是可疑致癌物.下列关于邻苯二甲酸二乙酯(结构如图所示)的说法不正确的是( )| A、不溶于水,可溶于乙醇、醋酸等有机溶剂 |
| B、既能发生加成反应,也能发生取代反应 |
| C、1mol该物质恰好能与2mol NaOH完全反应 |
| D、0.1mol该物质充分燃烧需要标准状况的氧气32L |