题目内容
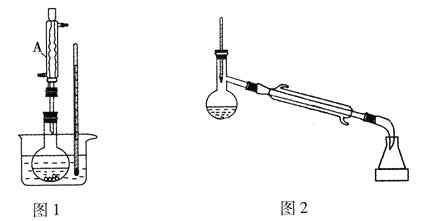
【题目】下图是一个实验室制取氯气并以氯气为原料进行一系列反应的装置,回答下列问题。
(1)写出a仪器的名称_______;
(2)装置D产生白色沉淀现象的原因_______________________;
(3)E装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为CO2和HCl。试写出E中反应的化学方程式_________________________________;
(4)F处的烧杯溶液中最终____(填“有”或“没有”)白色沉淀;
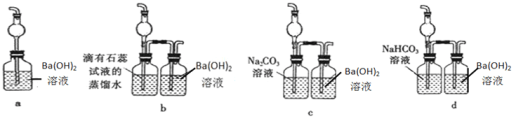
(5)F装置无法确认E处反应中有CO2产生,为了证明CO2的存在,要对F装置进行改造,装置符合要求的是_____________。
【答案】分液漏斗 氯气将二氧化硫在水中氧化成硫酸,硫酸与氯化钡反应生成白色的硫酸钡沉淀 ![]() 没有 b
没有 b
【解析】
(1)根据仪器a的构造判断其名称;
(2)Cl2+SO2+2H2O=2HCl+H2SO4,生成的硫酸再与氯化钡反应生成白色的硫酸钡沉淀来分析;
(3)氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应;
(4)氯化氢、氯气和澄清石灰水反应都生成的盐和水;
(5)确认E处反应中有CO2产生,需用澄清的石灰水变浑浊验证,需除去二氧化碳中的氯化氢、氯气,且不能生成二氧化碳;
:(1)根据仪器的构造可知a为分液漏斗;
故答案为:分液漏斗;
(2)E装置产生白色沉淀现象的原因是氯气和二氧化硫发生氧化还原反应,即Cl2+SO2+2H2O=2HCl+H2SO4生成的硫酸又与氯化钡反应生成白色的硫酸钡沉淀;
故答案为:氯气将二氧化硫在水中氧化成硫酸,硫酸与氯化钡反应生成白色的硫酸钡沉淀;
(3)氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应生成氯化氢和二氧化碳,反应方程式为:![]() ,
,
故答案为:![]()
(4)剩余的氯气在F装置中和水反应生成盐酸和次氯酸,装置E中反应也生成氯化氢气体,氯化氢、氯气和澄清石灰水反应都生成可溶性的盐和水,二氧化碳的物质的量少于氯化氢,不可能生成碳酸钙沉淀,所以反应过程无现象无白色沉淀生成;
故答案为:没有
(5)因通入F装置的气体中含有氯气、氯化氢、二氧化碳,现需除去氯气和氯化氢,且除去这两种气体过程中不能产生二氧化碳,
装置a氯气、氯化氢、二氧化碳一同通入无法确认E处反应中有CO2产生;
装置d氯化氢与碳酸氢钠反应生成二氧化碳,无法确认E处反应中有CO2产生;
装置c中碳酸钠与氯化氢及氯气反应生生成二氧化碳,且碳酸钠溶液能吸收二氧化碳,无法确认E处反应中有CO2产生;
装置b中,少量氯气能溶于水,氯化氢极易溶于水,二氧化碳混有氯化氢时,二氧化碳在水中几乎不溶,用水可除去氯气和氯化氢两种气体,多余的气体与澄清石灰水作用变浑浊,能确认E处反应中有CO2产生,
故答案为:b。

 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案