题目内容
【题目】已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且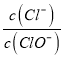 的值与温度高低有关。当n (KOH)=a mol时,下列有关说法错误的是
的值与温度高低有关。当n (KOH)=a mol时,下列有关说法错误的是
A.若某温度下,反应后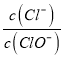 =11,则溶液中
=11,则溶液中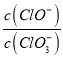 =
=![]()
B.参加反应的氯气的物质的量等于![]() a mol
a mol
C.改变温度,反应中转移电子的物质的量n的范围:![]() a mol ≤ n(e -)≤
a mol ≤ n(e -)≤![]() a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为 ![]() a mol
a mol
【答案】D
【解析】
A.假设n(ClO-)=1mol,则n(Cl-)=11mol,根据电子转移守恒计算n(ClO3-);
B.根据元素的原子守恒分析解答;
C.氧化产物只有KClO3时,转移电子最多,根据电子转移守恒n(KCl)=5n(KClO3),由钾离子守恒:n(KCl)+n(KClO3)=n(KOH);氧化产物只有KClO时,转移电子最少,根据电子转移守恒n(KCl)=n(KClO),根据钾离子守恒:n(KCl)+n(KClO)=n(KOH),进而计算转移电子物质的量范围;
D.氧化产物只有KClO3时,其物质的量最大,由钾离子守恒:n(KCl)+n(KClO3)=n(KOH),结合电子转移守恒计算。
A.假设n(ClO-)=1mol,由于反应后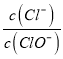 =11,则n(Cl-)=11mol,根据电子转移守恒可得5n(ClO3-)+n(ClO-)= n(Cl-),5×n(ClO3-)=11mol-1mol=10mol,所以n(ClO3-)=2mol,故溶液中
=11,则n(Cl-)=11mol,根据电子转移守恒可得5n(ClO3-)+n(ClO-)= n(Cl-),5×n(ClO3-)=11mol-1mol=10mol,所以n(ClO3-)=2mol,故溶液中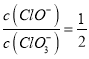 ,A正确;
,A正确;
B.由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+ n(KClO)+n(KClO3)=n(KOH),两式联立可得n(Cl2)=![]() n(KOH)=
n(KOH)=![]() ×a mol=
×a mol=![]() a mol,B正确;
a mol,B正确;
C.氧化产物只有KClO3时,转移电子最多,根据电子转移守恒n(KCl)=5n(KClO3),由钾离子守恒:n(KCl)+n(KClO3)=n(KOH),故n(KClO3)=![]() n(KOH)=
n(KOH)=![]() ×a mol=
×a mol=![]() a mol;转移电子最大物质的量为:
a mol;转移电子最大物质的量为:![]() a mol×5=
a mol×5=![]() a mol;
a mol;
氧化产物只有KClO时,转移电子最少,根据电子转移守恒n(KCl)=n(KClO),根据钾离子守恒:n(KCl)+n(KClO)=n(KOH),所以有n(KClO)=![]() n(KOH)=
n(KOH)=![]() ×a mol=
×a mol=![]() a mol,转移电子最小物质的量=
a mol,转移电子最小物质的量=![]() ×a mol×1=
×a mol×1=![]() a mol,则反应中转移电子的物质的量n(e-)的范围为:
a mol,则反应中转移电子的物质的量n(e-)的范围为:![]() a mol ≤ n(e -)≤
a mol ≤ n(e -)≤![]() a mol,C正确;
a mol,C正确;
D.氧化产物只有KClO3时,其物质的量最大,根据电子转移守恒n(KCl)=5n(KClO3),由钾离子守恒:n(KCl)+n(KClO3)=n(KOH),故n最大(KClO3)=![]() n(KOH)=
n(KOH)=![]() ×a mol=
×a mol=![]() a mol,D错误;
a mol,D错误;
故合理选项是D。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】苯甲醛在医药、染料、香料等行业有着广泛的应用。实验室通过如图所示的流程由甲苯氧化制备苯甲醛。
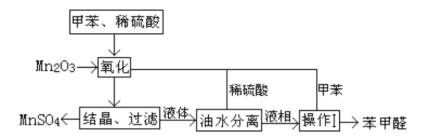
试回答下列问题:
(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是___。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的___。
(3)实验过程中,可循环使用的物质分别为___,___。
(4)实验中分离甲苯和苯甲醛采用的操作I是___________。
(5)实验中发现,反应时间不同苯甲醛的产率也不同(数据见下表),
反应时间/h | 1 | 2 | 3 | 4 | 5 |
苯甲醛产率/% | 76.0 | 87.5 | 83.6 | 72.5 | 64.8 |
请结合苯甲醛的结构,分析当反应时间过长时,苯甲醛产率下降的原因___。