题目内容
16.下列叙述中正确的是( )| A. | 周期表中第VA族元素的最高价氧化物对应水化物的化学式均为H3RO4 | |
| B. | O22-与S2-具有相同的质子数和电子数 | |
| C. | 所有主族元素的简单离子所带电荷数与其族序数相等 | |
| D. | 氕化锂、氘化锂、氚化锂可以作为“长征2号”火箭发射的重要燃料,LiH、LiD、LiT的化学性质不同 |
分析 A、ⅤA族元素,最高价为+5价,N元素的最高价氧化物对应水化物的化学式为HNO3;
B、O22-与S2-的质子数均为16和电子数均为18;
C、阴离子所带电荷数不一定等于其族序数;
D、H、D、T核外同位素,LiH、LiD、LiT的化学性质几乎完全相同.
解答 解:A、ⅤA族元素,最高价为+5价,N元素的最高价氧化物对应水化物的化学式为HNO3,故A错误;
B、O22-与S2-的质子数16和电子数为18,所以两种微粒具有相同的质子数和电子数,故B正确;
C、阴离子所带电荷数不一定等于其族序数,如:S2-、Cl-,故C错误;
D、H、D、T核外同位素,LiH、LiD、LiT的化学性质几乎完全相同,故D错误,
故选B.
点评 本题考查原子结构与性质,难度不大,注意C选项中阴离子所带电荷数可能等于其族序数,如氢负离子,D选项中三种化学式表示的物质实质是一种物质.

练习册系列答案
相关题目
17.设NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 2.24L CO2中含有的原子数为0.3NA | B. | 20g D2O所含的中子数为10NA | ||
| C. | 16g CH4中含C-H键数目为NA | D. | 1 mol 氦气含有的原子数为2NA |
7.下列各表为周期表的一部分(表中为原子序数),其中正确的是( )
| A. |
| B. |
| C. |
| D. |
|
4.下列物质中,既有离子键,又有共价键的是( )
| A. | CaCl2 | B. | Na2O | C. | H2SO4 | D. | NH4Cl |
11.某元素原子最外层只有1个电子,它跟氯元素相结合时,所形成的化学键是( )
| A. | 一定是共价键 | B. | 一定是离子键 | ||
| C. | 可能是共价键,也可能是离子键 | D. | 可能不形成化学键 |
8.变黑的银器可根据电化学原理进行翻新,其方法如下:在铝制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后黑色会褪去,该反应的化学方程式为:2Al+3Ag2S+6H2O=6Ag+3H2S↑+2Al(OH)3.下列关于说法正确的是( )
| A. | 正极反应式:Al-3e-+3H2O=Al(OH)3+3H+ | |
| B. | 放电过程中,Cl-向正极移动 | |
| C. | 每转移0.2mol电子,理论上生成0.1molH2S气体 | |
| D. | 处理过程中银器一直保持恒重 |
6.在100mL1mol•L-1 AlCl3溶液中滴加1mol•L-1NaOH溶液,得到3.9g沉淀,则加入的NaOH溶液的体积可能是( )
| A. | 160mL | B. | 200mL | C. | 300mL | D. | 350mL |
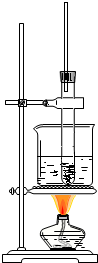 硝基苯是制造染料的重要原料.某同学在实验室里用右图装置制取硝基苯,主要步骤如下:
硝基苯是制造染料的重要原料.某同学在实验室里用右图装置制取硝基苯,主要步骤如下: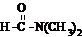 溶于水
溶于水