��Ŀ����
����Ŀ������ʱ����0.1 mol Fe(NO3)3��2 mol HCl����ˮ�õ�2L�����Һ��Ȼ�������Һ��Ͷ��m g���ۣ���ַ�Ӧ�μ�KSCN��Һ�����ɫ�������й�˵����ȷ����
A.���������ԣ�Fe3+>H+�������ȷ����ķ�Ӧ��Fe+2Fe3+=3Fe2+
B.��ַ�Ӧ������56 g��
C.m=28ʱ����Һʣ��0.9 mol H+
D.������16.8 g����ʱ�������ɱ�״����6.72 L����
���𰸡�D
��������
��������������������¾���ǿ�����ԣ���������Һ�м������ۺ��ȷ�����Ӧ��Fe+4H++NO3-=Fe3++NO��+2H2O��0.1 mol�������к���0.3 mol NO3-�����ݷ�Ӧ��֪��0.3 mol NO3-��ȫ��Ӧ����1.2 mol H+��ͬʱ����0.3 mol NO���壬H+��ʣ��0.8mol����ʱ��Һ�к���Fe3+�����ʵ���Ϊ��0.1 mol+0.3 mol=0.4 mol��Ȼ������Ӧ��Fe+2Fe3+=3Fe2+���������Ӧ��Fe+2H+=Fe2++H2�����ݴ˽���������ݽ��м��㡣
A. ��Һ�к���H+��NO3-���������Դ���Fe3+���������ȷ�����Ӧ��Fe+4H++NO3-=Fe3++NO��+2H2O��A����
B. ��ǰ������Ӧ������Fe�����ʵ���Ϊ��n(Fe)=n(NO3-)+![]() n��(Fe3+)=0.3 mol+0.4 mol��
n��(Fe3+)=0.3 mol+0.4 mol��![]() =0.5 mol����ʱ��Һ�л���ʣ��H+�����ʵ���Ϊ2 mol-4��0.3 mol=0.8 mol��������Ӧ��Fe+2H+=Fe2++H2��������Fe�����ʵ���Ϊ0.8 mol��
=0.5 mol����ʱ��Һ�л���ʣ��H+�����ʵ���Ϊ2 mol-4��0.3 mol=0.8 mol��������Ӧ��Fe+2H+=Fe2++H2��������Fe�����ʵ���Ϊ0.8 mol��![]() =0.4 mol�����Է�Ӧ�����ĵ��������ʵ���Ϊ0.5 mol+0.4 mol=0.9 mol����Ӧ����Fe������Ϊ��0.9mol��56 g/mol=5.04g��B����
=0.4 mol�����Է�Ӧ�����ĵ��������ʵ���Ϊ0.5 mol+0.4 mol=0.9 mol����Ӧ����Fe������Ϊ��0.9mol��56 g/mol=5.04g��B����
C. ����ѡ��B�����֪����Ͷ������28gʱ��ֻ����ǰ������Ӧ����ʱʣ��H+�����ʵ���Ϊ0.8 mol��C����
D. 16.8 g Fe�������ʵ���Ϊ��n(Fe)=![]() =0.3 mol�����ݷ�ӦFe+4H++NO3-=Fe3++NO��+2H2O��֪��0.3 mol����ȫ��Ӧ����0.3 molNO���壬���ڱ�״�������ΪV(NO)=0.3mol��22.4L/mol=6.72 L��D��ȷ��
=0.3 mol�����ݷ�ӦFe+4H++NO3-=Fe3++NO��+2H2O��֪��0.3 mol����ȫ��Ӧ����0.3 molNO���壬���ڱ�״�������ΪV(NO)=0.3mol��22.4L/mol=6.72 L��D��ȷ��
�ʺ���ѡ����D��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��ʵ���ҴӺ����Һ![]() ����
����![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() �л��յ⣬�����������£�
�л��յ⣬�����������£�

![]() ���Һ�м���
���Һ�м���![]() ��Һ����������ԭ����Ӧ�����ӷ���ʽΪ ______��
��Һ����������ԭ����Ӧ�����ӷ���ʽΪ ______��
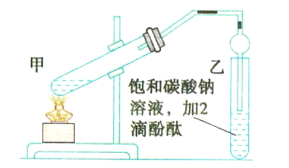
![]() ��������������������ƿ�н��У�����Һ���������pHԼΪ2������ͨ��
��������������������ƿ�н��У�����Һ���������pHԼΪ2������ͨ��![]() ��ʵ����ˮԡ������
��ʵ����ˮԡ������![]() ���ҵĽϵ��¶��½��е�ԭ���� ______��
���ҵĽϵ��¶��½��е�ԭ���� ______��

![]() ij�о�С����ͼװ�ö�
ij�о�С����ͼװ�ö�![]() ��KI��Һ�ķ�Ӧ����̽��������ͨ��
��KI��Һ�ķ�Ӧ����̽��������ͨ��![]() һ��ʱ���KI��Һ��Ϊ��ɫ������ͨ��
һ��ʱ���KI��Һ��Ϊ��ɫ������ͨ��![]() ������Һ��ɫ��dz������Ϊ��ɫ���о�С���������ɫ��Һ�е�Ԫ�صĴ�����̬��������¼��裺
������Һ��ɫ��dz������Ϊ��ɫ���о�С���������ɫ��Һ�е�Ԫ�صĴ�����̬��������¼��裺

����һ��û��![]() ��̬���������û��
��̬���������û��![]() ��̬������������
��̬������������![]() ��̬��
��̬��
![]() �����ʵ��֤������һ����
�����ʵ��֤������һ����![]() �Լ���ѡ
�Լ���ѡ![]() ��
��
ʵ����� | Ԥ������ | ���� |
_______ | _______ | ����һ���� |
![]() ���������������������
����������������д������![]() �����ӷ���ʽ ______��
�����ӷ���ʽ ______��
![]() ���о�С�黹�����˶Լӵ�����
���о�С�黹�����˶Լӵ�����![]() �����ⶨ������ʵ�飺
�����ⶨ������ʵ�飺
![]() ȷ��ȡ�ӵ���mg���ձ��У�������������ˮ������KI���ٵ���������ϡ���ᣬ��ַ�Ӧ�������û��Һ���
ȷ��ȡ�ӵ���mg���ձ��У�������������ˮ������KI���ٵ���������ϡ���ᣬ��ַ�Ӧ�������û��Һ���![]() ������Һ����ȡ
������Һ����ȡ![]() ������Һ����ƿ�У��Ӽ��ε�����Һ����c
������Һ����ƿ�У��Ӽ��ε�����Һ����c![]()
![]() ��Һ�ζ����յ㣬�ظ�3�Σ����ƽ��ֵΪVmL��
��Һ�ζ����յ㣬�ظ�3�Σ����ƽ��ֵΪVmL��
��֪��![]() ��
��![]() ���ⶨʱ���жϴﵽ�ζ��յ������Ϊ ______ ���ɲⶨ���ݿ���ø���Ʒ�к�
���ⶨʱ���жϴﵽ�ζ��յ������Ϊ ______ ���ɲⶨ���ݿ���ø���Ʒ�к�![]() ����������Ϊ ______
����������Ϊ ______ ![]() �ú�m��c��V�Ĵ���ʽ��ʾ��
�ú�m��c��V�Ĵ���ʽ��ʾ��![]()
![]() ��
��
![]() �ڵζ�������ȷ���������£��ô��ֲⶨ������õĽ������ƫ�ߣ���ԭ�����ܿ�����Ӱ�죬�������ӷ���ʽ��ʾ������һӰ���ԭ�� ______��
�ڵζ�������ȷ���������£��ô��ֲⶨ������õĽ������ƫ�ߣ���ԭ�����ܿ�����Ӱ�죬�������ӷ���ʽ��ʾ������һӰ���ԭ�� ______��