题目内容
【题目】(1) 写出CO2的空间构型:___________。
(2) 写出Na3N的电子式:____________________。
(3) 写出C2H6O的化学名称:______________________。
(4) 写出乙烯的实验式:_________________。
【答案】直线形 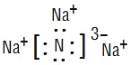 乙醇或二甲醚 CH2
乙醇或二甲醚 CH2
【解析】
(1) CO2分子的结构式为O=C=O,中心原子碳的最外层没有孤对电子,三个原子位于一条直线上;
(2) Na3N由Na+和N3-通过离子键相结合;
(3) C2H6O的分子结构可能是CH3CH2OH,也可能是CH3OCH3;
(4)乙烯的分子式为C2H4,实验式就是最简式。
(1) CO2的结构式为O=C=O,中心原子碳的最外层没有孤对电子,三个原子位于一条直线上,则其空间构型为直线形;答案为:直线形;
(2) Na3N由Na+和N3-通过离子键相结合,则其电子式为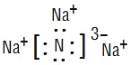 ;答案为:
;答案为: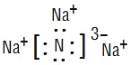 ;
;
(3) C2H6O的分子结构可能是CH3CH2OH,也可能是CH3OCH3;化学名称为乙醇或二甲醚;答案为:乙醇或二甲醚;
(4) 乙烯的分子式为C2H4,实验式就是最简式,则其实验式为CH2;答案为:CH2。

 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】工业上先将煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:CO(g)+H2O(g)CO2(g)+H2(g)。
(1)平衡常数的表达式K=_________________________
(2)向1L恒容密闭容器中充入CO和H2O(g),某温度时测得部分数据如下表。
t/min | 0 | 1 | 2 | 3 | 4 |
n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
则从反应开始到2min时,用H2表示的反应速率为__________;该温度下反应的平衡常数K=________(小数点后保留2位有效数字)。
(3)已知该反应在不同的温度下的平衡常数数值分别为
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.19 | 1.00 | 0.60 | 0.38 |
①根据表中的数据判断,该反应为________(填“吸热”或“放热”)反应。
②800℃,向2L恒容密闭容器中充入1molCO(g)、1molH2O(g)、2molCO2(g)、2molH2(g),此时v正_______v逆 (填“>”“<”或“=”)。