题目内容
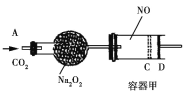
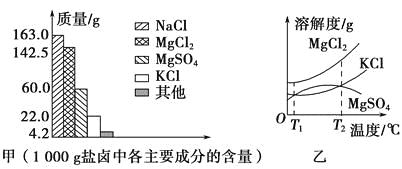
【题目】我国拥有很长的海岸线,具有丰富的海洋资源,以海水为原料的盐化工是我国重要的产业。盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如下图甲)。盐卤在食品、化工等方面具有广泛的用途。请解答下列与盐卤有关的试题。
(1)根据图甲,写出盐卤中含量最多的两种盐的化学式:_______、_______。
(2)下图乙是盐卤中某些物质的溶解度曲线,已知T1℃时,MgSO4和KCl的溶解度分别为M、N,则它们溶解度大小的关系为_______;将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是______________________________________________________。
(3)化工厂利用卤水生产金属镁的工艺流程如下:
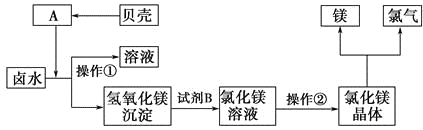
“操作①”的目的是将氢氧化镁沉淀分离出来,操作①的名称是_______。氢氧化镁与试剂B反应的化学方程式为______________________________。
操作②的名称是_______。该方法的优点为___________________________。
(4)用电解法制备金属镁,两位同学分别设计了下面的两种方法。
甲:电解氯化镁溶液。
乙:电解熔融的氯化镁。
其中同学_______(填“甲”或“乙”)能够成功地制备金属镁,假设生产过程中镁元素没有损失,则100 g卤水可制备镁_______g。
【答案】NaCl MgCl2 相等 MgSO4 过滤 Mg(OH)2+2HCl=MgCl2+2H2O 蒸发、结晶 就地取材,节约资源,降低成本 乙 4.8
【解析】
(1)从甲图中可以看出1 000 g盐卤中含有的NaCl、MgCl2、MgSO4、KCl分别为163.0 g、142.5 g、60.0 g、22.0 g,由此可见,含量最多的两种盐是NaCl、MgCl2。
(2)在T1℃时,KCl和MgSO4的溶解度曲线相交,说明T1℃时,二者的溶解度相等;T2℃以后,MgSO4的溶解度随着温度的升高而降低,故升高到一定温度时会析出。
(3)分离固体与液体的混合物应用过滤方法,而使溶液中的溶质以晶体的形式析出则需要蒸发、结晶。由于就地选用了海边的贝壳为原料来生产CaO,所以节约了资源,降低了生产成本。
(4)制备金属镁应该电解熔融的MgCl2,如果电解氯化镁溶液得到的不是镁,而是氢气、氯气和Mg(OH)2;根据卤水中镁原子的守恒,可以得出电解所得到的镁的质量为100 g×![]() ×
×![]() +100 g×
+100 g×![]() ×
×![]() =3.6 g+1.2 g=4.8 g。
=3.6 g+1.2 g=4.8 g。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案【题目】A~H八种短周期主族元素在周期表中的相对位置如图所示,已知C元素形成的单质有“国防金属”的美誉,![]() 的最高化合价与最低化合价之和为2。回答下列问题:
的最高化合价与最低化合价之和为2。回答下列问题:
A | …… | D | E | F | ||
B | C | …… | G | H |
(1)D元素在周期表中的位置为________________。
(2)上述元素所形成的气态单质中能用于饮用水消毒的有________________(填化学式)。
(3)B的单质在F的单质中燃烧的火焰颜色为________。
(4)C元素的单质可以在D和F形成的一种气态化合物中燃烧,写出该反应的化学方程式_____